题目内容
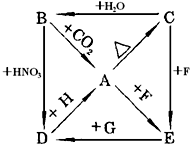 A、B、C、D、E五种物质都是含二价金属元素X的化合物,它们之间存在下列转化关系,图中H,G,F为另加的试剂.根据以上关系回答:
A、B、C、D、E五种物质都是含二价金属元素X的化合物,它们之间存在下列转化关系,图中H,G,F为另加的试剂.根据以上关系回答:(1)写出有关物质的化学式:
B
(2)写出D→A,E→D,A→E的离子方程式:
D→A
E→D
A→E
考点:无机物的推断
专题:推断题
分析:A、B、C、D、E五种物质都是含二价金属元素X的化合物,A加热能生成C,C和水反应生成B,B和二氧化碳生成A,假设A是碳酸钙,则C使CaO,氧化钙和水反应生成B为氢氧化钙,B和硝酸反应生成D,D应为硝酸钙,D和H反应生成A,A为碳酸钙,那么H是可溶性碳酸盐,假设为碳酸钠,氧化钙和碳酸钙均与F反应生成E,则F为盐酸,E为氯化钙,氯化钙与G反应生成硝酸钙,则G为硝酸银,带入验证即可.
解答:
解:A、B、C、D、E五种物质都是含二价金属元素X的化合物,A加热能生成C,C和水反应生成B,B和二氧化碳生成A,假设A是碳酸钙,则C使CaO,氧化钙和水反应生成B为氢氧化钙,B和硝酸反应生成D,D应为硝酸钙,D和H反应生成A,A为碳酸钙,那么H是可溶性碳酸盐,假设为碳酸钠或碳酸钾,氧化钙和碳酸钙均与F反应生成E,则F为盐酸,E为氯化钙,氯化钙与G反应生成硝酸钙,则G为硝酸银,
(1)由以上分析知B为Ca(OH)2,C为CaO,F为HCl,G为AgNO3,H为Na2CO3或K2CO3,故答案为:Ca(OH)2;CaO;HCl;AgNO3;Na2CO3或K2CO3;
(2)硝酸钙生成碳酸钙反应离子方程式为CO32-+Ca2+=CaCO3↓,
氯化钙生成硝酸钙反应的离子方程式为Cl-+Ag+=AgCl↓,
碳酸钙生成氯化钙反应的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:CO32-+Ca2+=CaCO3↓;Cl-+Ag+=AgCl↓;CaCO3+2H+=Ca2++CO2↑+H2O.
(1)由以上分析知B为Ca(OH)2,C为CaO,F为HCl,G为AgNO3,H为Na2CO3或K2CO3,故答案为:Ca(OH)2;CaO;HCl;AgNO3;Na2CO3或K2CO3;
(2)硝酸钙生成碳酸钙反应离子方程式为CO32-+Ca2+=CaCO3↓,
氯化钙生成硝酸钙反应的离子方程式为Cl-+Ag+=AgCl↓,
碳酸钙生成氯化钙反应的离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:CO32-+Ca2+=CaCO3↓;Cl-+Ag+=AgCl↓;CaCO3+2H+=Ca2++CO2↑+H2O.
点评:本题考查了物质性质的转化关系的分析推断,物质性质的掌握和反应特征是解题关键,题目难度中等.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
除去混合物中的杂质(括号中为杂质),所选试剂和分离方法都正确的是( )
| 混合物 | 除杂试剂 | 分离方法 | |
| A | 溴苯(溴) | NaOH溶液 | 分液 |
| B | 乙烷(乙烯) | 酸性KMnO4 | 洗气 |
| C | 甲苯(苯酚) | 溴水 | 过滤 |
| D | 溴乙烷(乙醇) | NaOH溶液 | 分液 |
| A、A | B、B | C、C | D、D |
将HBr(g)充入恒容密闭容器,恒温下发生反应2HBr(g)?H2(g)+Br2(g)△H>0,平衡时HBr(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时HBr(g)的转化率为b.下列a与b关系正确的是( )
| A、a>b | B、a=b |
| C、a<b | D、无法确定 |
在下列变化中,需要加入合适的氧化剂才能实现的是( )
| A、Na2O2→O2 |
| B、CO2→CO |
| C、Fe2O3→Fe |
| D、Br-→Br2 |
主族元素M、R形成的简单离子M2-离子与R+离子的核外电子数之和为20,下列说法正确的是( )
| A、M与R的原子序数之差可能等于7 |
| B、若M在第3周期,则R一定在第2周期 |
| C、M2-的离子半径可能比R+的离子半径小 |
| D、两种离子结合形成的化合物可能是共价化合物 |
关于化学反应的△H的理解正确的是( )
| A、△H>0的反应是吸热反应 |
| B、△H=ΣH(反应物)-ΣH(生成物) |
| C、所有化学反应的△H都可以通过实验测出 |
| D、△H=反应中化学键形成时吸收的总能量-反应中化学键断裂时放出的总能量 |