题目内容
5.已知:2Fe+3Br2═2FeBr3,Fe2+的还原性大于Br-现有16.8g铁和0.3molBr2反应后加入适量水后,通入amolCl2.(1)当a≤0.15时,反应离子方程式为2Fe2++Cl2═2Fe3++2Cl-
(2)当Fe2+与Br-同时被氧化时,a的取值范围为0.15<a
(3)当a=0.3时,反应后氧化产物与还原产物的物质的量之比为9:4.
分析 n(Fe)=$\frac{16.8g}{56g/mol}$=0.3mol,n(Br2)=0.3mol,由反应2Fe+3Br2═2FeBr3可知,反应后Fe过量,在溶液中进一步发生Fe+2Fe3+=3Fe2+,则反应后溶液中存在0.3molFe2+和0.6molBr-,结合Fe2+的还原性大于Br-解答该题.
解答 解:(1)当a≤0.15时,氯气不足,因Fe2+的还原性大于Br-,只发生2Fe2++Cl2═2Fe3++2Cl-,故答案为:2Fe2++Cl2═2Fe3++2Cl-;
(2)因为反应后溶液中存在0.3molFe2+和0.6molBr-,所以当Fe2+完全被氧化时,则需要氯气为$\frac{0.3}{2}$=0.15mol,所以当Fe2+与Br-同时被氧化时,a的取值范围为0.15<a,故答案为:0.15<a;
(3)当a=0.3时,首先发生2Fe2++Cl2═2Fe3++2Cl-,此时Fe2+完全反应,消耗0.15molCl2,又知Br-为0.6mol,剩余氯气为0.15mol,发生2Br-+Cl2═Br2+2Cl-,则总反应为方程式6FeBr2+6Cl2=4FeCl3+2FeBr3+3Br2,则反应后氧化产物(4FeCl3+2FeBr3+3Br2)与还原产物(4FeCl3)的物质的量之比为9:4,故答案为:9:4.
点评 本题考查氧化还原反应中氧化性和还原性强弱的知识,综合性较强,题目难度较大,解答本题时注意根据离子的还原性强弱判断反应的先后顺序和各离子的物质的量,为解答该题的关键,也是易错点,答题时注意体会.

练习册系列答案
相关题目
13.相等物质的量的CO和CO2,下列比较中正确的是( )
①所含的分子数目之比为1:1 ②所含的氧原子数目之比为1:2
③所含的碳原子数目之比为1:1 ④所含的原子总数目之比为2:3.
①所含的分子数目之比为1:1 ②所含的氧原子数目之比为1:2
③所含的碳原子数目之比为1:1 ④所含的原子总数目之比为2:3.
| A. | ①② | B. | ②③ | C. | ①②③ | D. | ①②③④ |
20.要除去下列四种物质中的少量杂质(括号内物质为杂质).
甲:炭粉(氧化铜) 乙:NaOH(Na2CO3) 丙:KCl(KHCO3) 丁:CaCO3(Na2CO3)
可选用的试剂及操作方法有:
①加适量盐酸,搅拌,过滤; ②加适量水,搅拌,过滤③加适量盐酸,蒸发; ④溶解,加适量石灰水,过滤,蒸发
下列组合正确的是( )
甲:炭粉(氧化铜) 乙:NaOH(Na2CO3) 丙:KCl(KHCO3) 丁:CaCO3(Na2CO3)
可选用的试剂及操作方法有:
①加适量盐酸,搅拌,过滤; ②加适量水,搅拌,过滤③加适量盐酸,蒸发; ④溶解,加适量石灰水,过滤,蒸发
下列组合正确的是( )
| A. | 甲-②,乙-④ | B. | 乙-③,丙-③ | C. | 乙-④,丁-② | D. | 丙-①,丁-② |
10.实验室保存下列物质的方法中,正不确的是( )
| A. | 少量金属钠保存在水里 | |
| B. | 澄清石灰水需盛放在用橡皮塞塞紧的试剂瓶中 | |
| C. | 为了防止Fe2+被氧化,可在盛FeSO4溶液的试剂瓶中加少量铁粉 | |
| D. | 新制氯水通常保存在棕色试剂瓶中 |
17.下列说法正确的是( )
| A. | 二氧化碳溶于水能部分电离,故二氧化碳属于电解质 | |
| B. | 硫酸钡难溶于水,但硫酸钡属于强电解质 | |
| C. | 氯化钠溶液在电流作用下完全电离成钠离子和氯离子 | |
| D. | 强电解质溶液的导电性一定比弱电解质溶液的导电性强 |
14.硅及其化合物在材料领域中应用广泛.下列叙述中,正确的是( )
| A. | 用带玻璃瓶塞的试剂瓶盛放NaOH溶液 | |
| B. | 硅是地壳中含量最多的元素 | |
| C. | SiO2不溶于水,也不溶于任何酸 | |
| D. | 晶体硅是良好的半导体材料 |
15.如图是某同学用500mL容量瓶配制0.10mol•L-1 Na2CO3溶液的步骤:该同学的错误是( )
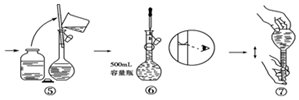

| A. | ⑤⑥ | B. | ⑦ | C. | ⑥ | D. | ⑤⑥⑦ |