题目内容
在BaCl2溶液中通入下列气体后,溶液中一定会出现白色沉淀的是( )
| A、SO2 |
| B、先通NO2,后通SO2 |
| C、先通SO2,后通H2S |
| D、NH3,CO2 |
考点:氮的氧化物的性质及其对环境的影响,弱电解质在水溶液中的电离平衡
专题:元素及其化合物
分析:A、氯化钡溶液和二氧化硫气体不反应;
B、先通NO2和水反应生成硝酸和一氧化氮,硝酸具有强氧化性能氧化后通入的SO2 为硫酸,硫酸和氯化钡反应生成硫酸钡沉淀;
C、先通SO2,后通H2S,反应生成淡黄色沉淀;
D、通入NH3,反应生成一水合氨,再通入CO2 会反应生成碳酸铵,遇到氯化钡反应生成碳酸钡白色沉淀;
B、先通NO2和水反应生成硝酸和一氧化氮,硝酸具有强氧化性能氧化后通入的SO2 为硫酸,硫酸和氯化钡反应生成硫酸钡沉淀;
C、先通SO2,后通H2S,反应生成淡黄色沉淀;
D、通入NH3,反应生成一水合氨,再通入CO2 会反应生成碳酸铵,遇到氯化钡反应生成碳酸钡白色沉淀;
解答:
解:A、氯化钡溶液和二氧化硫气体不反应,无白色沉淀生成,故A不符合;
B、先通NO2和水反应生成硝酸和一氧化氮,硝酸具有强氧化性能氧化后通入的SO2 为硫酸,硫酸和氯化钡反应生成硫酸钡沉淀,故B符合;
C、先通SO2,后通H2S,反应生成淡黄色沉淀,无白色沉淀生成,故C不符合;
D、通入NH3,反应生成一水合氨,再通入CO2 会反应生成碳酸铵,遇到氯化钡反应生成碳酸钡白色沉淀,故D符合;
故选BD.
B、先通NO2和水反应生成硝酸和一氧化氮,硝酸具有强氧化性能氧化后通入的SO2 为硫酸,硫酸和氯化钡反应生成硫酸钡沉淀,故B符合;
C、先通SO2,后通H2S,反应生成淡黄色沉淀,无白色沉淀生成,故C不符合;
D、通入NH3,反应生成一水合氨,再通入CO2 会反应生成碳酸铵,遇到氯化钡反应生成碳酸钡白色沉淀,故D符合;
故选BD.
点评:本题考查了物质性质的分析应用,主要是硝酸氧化性和氨气是碱性气体分析,掌握基础和物质性质是解题关键,题目难度中等.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
某物质在常温下为无色气体,但暴露在空气中后会立刻变为红棕色气体的是( )
| A、SO2 |
| B、NO |
| C、N2 |
| D、Cl2 |
80年代中期,科学家发现并证明碳还以新的单质形态C60存在.后来人们又相继得到了C70、C76、C84、C90、C94等另外一些球碳分子.90年代初,科学家又发现了管状碳分子和洋葱状碳分子(如图).下列说法错误的是( )
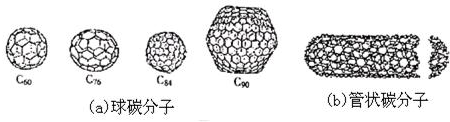

| A、金刚石和石墨的熔点肯定要比C60高 |
| B、据估计C60熔点比金刚石和石墨要高 |
| C、无论是球碳分子,还是管状碳分子、洋葱状碳分子,都应看作是碳的同素异形体 |
| D、球碳分子是碳的同素异形体 |
下列各组物质互为同分异构体的是( )
| A、H2O和H2O2 |
| B、己烷与环己烷 |
C、 与CH3CH2CH2CH3 与CH3CH2CH2CH3 |
| D、氰酸铵NH4CNO与尿素CO(NH2)2 |
有机物A的结构简式为 ,A的同分异构体中带苯环的化合物(烯醇结构除外)共有( )
,A的同分异构体中带苯环的化合物(烯醇结构除外)共有( )
 ,A的同分异构体中带苯环的化合物(烯醇结构除外)共有( )
,A的同分异构体中带苯环的化合物(烯醇结构除外)共有( )| A、3种 | B、4种 | C、5种 | D、6种 |
燃烧某混合气体,所产生的CO2的质量一定大于燃烧相同质量乙烯所产生的CO2的量,该混合气体是( )
| A、乙烯、丙烷 |
| B、苯、乙烯 |
| C、甲烷、丙烷 |
| D、乙烷、环丙烷(C3H6) |
下列各图均能表示甲烷的分子结构,哪一种更能反映其真实存在状况( )
A、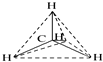 甲烷分子结构示意图 |
B、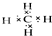 甲烷分子的电子式 |
C、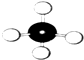 球棍模型 |
D、 比例模型 |
充分燃烧3L由甲烷、乙烯和丙炔组成的混合气体,生成7L CO2和4.82g水(气体体积均在标准状况下测定),则原混合气体中甲烷、乙烯和乙炔的体积比可能是( )
| A、1:1:1 |
| B、1:2:3 |
| C、3:2:1 |
| D、3:1:2 |
下列关于有机化学实验的说法正确的是( )
A、实验室制取乙烯的反应原理:C2H5OH
| |||
| B、实验室制取C2H2,一般用碳化钙跟饱和食盐水反应以适度减缓反应速率 | |||
| C、实验室分离苯和苯酚的混合物,可采用溴水 | |||
| D、由1-溴丁烷跟氢氧化钠醇溶液共热,可以制得两种烯烃 |