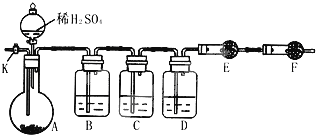
题目内容
某酸的酸式盐NaHY在水溶液中,HY-的电离程度小于HY-的水解程度.有关的叙述正确的是( )
| A、H2Y的电离方程式为:H2Y=2H++Y2- |
| B、在该酸式盐溶液中:[Na+]>[Y2-]>[HY-]>[OH-]>[H+] |
| C、HY-的水解方程式:HY-+H2O?H3O++Y2- |
| D、在该酸式盐溶液中:[Na+]>[HY-]>[OH-]>[H+]>[Y2-] |
考点:离子浓度大小的比较
专题:
分析:A.A、H2Y是二元弱酸,电离时分两步电离;
B.酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度,溶液呈酸性,据此判断各种离子浓度大小;
C.HY-水解生成二元弱酸和氢氧根离子;
D.酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度,溶液呈酸性,据此判断各种离子浓度大小.
B.酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度,溶液呈酸性,据此判断各种离子浓度大小;
C.HY-水解生成二元弱酸和氢氧根离子;
D.酸式盐NaHY的水溶液中,HY-的电离程度小于HY-的水解程度,溶液呈酸性,据此判断各种离子浓度大小.
解答:
解:A.H2Y是二元弱酸,电离时分两步电离,第一步电离生成氢离子和酸式酸根离子,电离方程式为:H2Y+H2O?HY-+H3O+,故A错误;
B.NaHY的水溶液中,阴离子水解,钠离子不水解,所以c(Na+)>c(HY-);HY-的电离程度小于HY-的水解程度,但无论电离还是水解都较弱,阴离子还是以HY-为主,溶液呈碱性,说明溶液中c(OH-)>c(H+);因溶液中还存在水的电离,则c(H+)>c(Y2-),所以离子浓度大小顺序为:[Na+]>[HY-]>[OH-]>[H+]>[Y2-],故B错误;
C.HY-水解生成二元弱酸和氢氧根离子,水解方程式为:HY-+H2O?HO-+H2Y,故C错误;
D.根据B的分析可知:[Na+]>[HY-]>[OH-]>[H+]>[Y2-],故D正确;
故选D.
B.NaHY的水溶液中,阴离子水解,钠离子不水解,所以c(Na+)>c(HY-);HY-的电离程度小于HY-的水解程度,但无论电离还是水解都较弱,阴离子还是以HY-为主,溶液呈碱性,说明溶液中c(OH-)>c(H+);因溶液中还存在水的电离,则c(H+)>c(Y2-),所以离子浓度大小顺序为:[Na+]>[HY-]>[OH-]>[H+]>[Y2-],故B错误;
C.HY-水解生成二元弱酸和氢氧根离子,水解方程式为:HY-+H2O?HO-+H2Y,故C错误;
D.根据B的分析可知:[Na+]>[HY-]>[OH-]>[H+]>[Y2-],故D正确;
故选D.
点评:本题考查了溶液中离子浓度大小比较,题目难度中等,明确“HY-的电离程度小于HY-的水解程度”的含义为解答本题的关键,注意掌握电荷守恒、物料守恒、盐的水解原理在判断溶液离子浓度大小中的应用方法.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
已知,mg Al在足量氯气中燃烧,生成固体的质量为(m+21.3)g,若将mgAl投入总质量为95.2g的NaOH水溶液中恰好完全反应,则所得溶液中溶质的质量分数为( )
| A、5.4% | B、8.0% |
| C、16.3% | D、16.4% |
NaCl晶体中钠和氯离子周围都是由六个相反离子按八面体形状排列的,解释这样的结构可以用( )
| A、杂化轨道 | B、键的极性 |
| C、离子大小 | D、离子电荷 |
 某烧碱溶液中含有少量杂质(不与盐酸反应),现用标准盐酸滴定NaOH溶液,测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用标准盐酸滴定NaOH溶液,测定其浓度.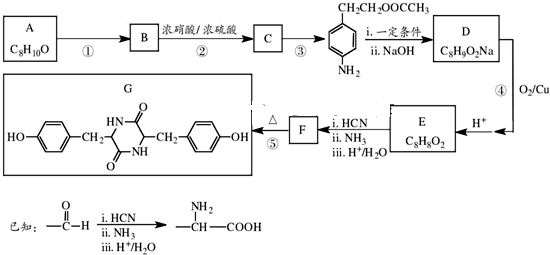
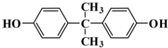 )与光气(
)与光气(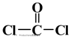 )聚合得到,请写出该聚碳酸酯的结构简式
)聚合得到,请写出该聚碳酸酯的结构简式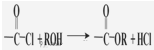 )
)