题目内容
20.分子式为C5H12的烷烃一共有多少种同分异构体( )| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
分析 烷烃可利用减链法书写同分异构体,有主链含5个C、4个C、3个C的同分异构体,以此来解答.
解答 解:分子式为C5H12的烷烃为CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、C(CH3)4,共3种,
故选B.
点评 本题考查烷烃的同分异构体的书写,为高频考点,把握减链法书写同分异构体为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
17.实验室中需要配制2mol/L的NaCl溶液480mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
| A. | 480mL 56.2g | B. | 500mL 58.5g | ||
| C. | 1000mL 58.5g | D. | 任意规格 56.2g |
11.下列所得溶液的物质的量浓度为0.1mol•L-1的是( )
| A. | 将0.1mol氨充分溶解在1L水中 | |
| B. | 将10g质量分数为98%的硫酸与990g水混合 | |
| C. | 将10mL•1mol•L-1的盐酸与90mL水充分混合 | |
| D. | 将25.0g胆矾(CuSO4•5H2O)溶于水配成1L溶液 |
8.在500g 0.2%的盐酸和500g 2%的盐酸中,分别加入2.3g钠,钠全部反应后,产生的气体( )
| A. | 在浓度大的盐酸中反应产生的气体多 | |
| B. | 一样多 | |
| C. | 在浓度小的盐酸中反应产生的气体多 | |
| D. | 由反应的剧烈程度决定 |
15.亚氯酸钠也是一种高效氧化剂、漂白剂,且能用作砂糖、食品生产的消毒剂,亚氯酸钠受热易分解,易溶于水.
(1)图1是生产亚氯酸钠的工艺流程图:

①写出Ⅱ的化学方程式ClO2+H2O2+2NaOH=2NaClO2+O2↑+2H2O
②操作Ⅰ包含C、E、过滤、洗涤
A.蒸发浓缩 B.蒸馏 C.减压蒸发浓缩 D.加热蒸发 E.冷却结晶 F.分液
(2)上述离子隔膜电解池的原理如图2,c、d为电极,ef、gh为离子交换膜,两膜中间的Na+和SO42-可通过隔膜,而两端隔室中离子被阻挡不能进入中间的隔室.
①c电极可以为B;
A.铁电极 B.石墨电极 C.铁或者石墨均可
②ef膜为阴离子交换膜(填“阳”或“阴”);
(3)亚氯酸钠漂白织物时真正起作用的是HClO2,表是25℃几种酸的电离平衡常数:
用亚氯酸钠漂白织物时,下列物质可以用作酸化剂的是c.
a.SO2 b.CO2 c.稀硫酸 d.盐酸 e.HClO.
(1)图1是生产亚氯酸钠的工艺流程图:

①写出Ⅱ的化学方程式ClO2+H2O2+2NaOH=2NaClO2+O2↑+2H2O
②操作Ⅰ包含C、E、过滤、洗涤
A.蒸发浓缩 B.蒸馏 C.减压蒸发浓缩 D.加热蒸发 E.冷却结晶 F.分液
(2)上述离子隔膜电解池的原理如图2,c、d为电极,ef、gh为离子交换膜,两膜中间的Na+和SO42-可通过隔膜,而两端隔室中离子被阻挡不能进入中间的隔室.
①c电极可以为B;
A.铁电极 B.石墨电极 C.铁或者石墨均可
②ef膜为阴离子交换膜(填“阳”或“阴”);
(3)亚氯酸钠漂白织物时真正起作用的是HClO2,表是25℃几种酸的电离平衡常数:
| 酸 | HClO2 | H2CO3 | HClO |
| Ka | 1×10-2 | K1=4.3×10-7、K2=5.6×10-11 | 3×10-8 |
a.SO2 b.CO2 c.稀硫酸 d.盐酸 e.HClO.
12.下列说法不正确的是( )
| A. | 碘酒可使蛋白质变性,故能消毒杀菌 | |
| B. | 天然氨基酸能溶于强酸或强碱溶液,在两性化合物 | |
| C. | 常温下,强酸和弱酸的浓度相同时,强酸中水的电离程度比弱酸中的大 | |
| D. | 船舶外壳装上锌块,是牺牲阳极的阴极保护法进行防腐 |
9.下列说法正确的是( )
| A. | 试纸在检测溶液时不需要湿润,而检测气体时必须湿润 | |
| B. | 焰色反应使用的铂丝通常可用稀硫酸清洗 | |
| C. | 碘水中的碘可以用酒精萃取 | |
| D. | 在实验室遇酸灼伤,用水洗后再用稀NaOH溶液浸洗 |
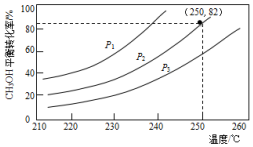 2016年9月.“乔歌里1号”中国首台静默移动发电站MFC30正式问世,MFC30是基于甲醇重整制氢燃料电池发电技术.
2016年9月.“乔歌里1号”中国首台静默移动发电站MFC30正式问世,MFC30是基于甲醇重整制氢燃料电池发电技术.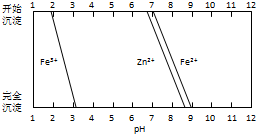 铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为:
铁酸锌(ZnFe2O4)是对可见光敏感的半导体催化剂,其实验室制备原理为: