题目内容
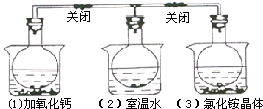 如图所示,三个烧瓶中分别充满NO2气体,并分别放置在盛有下列物质的烧杯中(烧杯内有水):在(1)中加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4Cl晶体,发现(1)中红棕色变深,(3)中红棕色变浅,下列叙述正确的是( )
如图所示,三个烧瓶中分别充满NO2气体,并分别放置在盛有下列物质的烧杯中(烧杯内有水):在(1)中加入CaO,在(2)中不加其他任何物质,在(3)中加入NH4Cl晶体,发现(1)中红棕色变深,(3)中红棕色变浅,下列叙述正确的是( )| A、烧瓶(3)中气体的压强增大 |
| B、NH4Cl溶于水时放出热量 |
| C、烧瓶(1)中平衡时混合气体的平均相对分子质量增大 |
| D、2NO2?N2O4是放热反应 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:三个烧瓶中都存在如下平衡:2NO2?N2O4;
(1)中红棕色变深,平衡左移,由于氧化钙反应放热,所以2NO2?N2O4反应放热;
(3)中变浅,平衡右移,说明氯化铵溶解吸热;
A、根据气体的物质的量变化判断;
B、根据(3)中气体颜色变化判断;
C、根据平衡移动方向对气体物质的量的影响判断;
D、根据(1)中混合气体颜色变化判断.
(1)中红棕色变深,平衡左移,由于氧化钙反应放热,所以2NO2?N2O4反应放热;
(3)中变浅,平衡右移,说明氯化铵溶解吸热;
A、根据气体的物质的量变化判断;
B、根据(3)中气体颜色变化判断;
C、根据平衡移动方向对气体物质的量的影响判断;
D、根据(1)中混合气体颜色变化判断.
解答:
解:A、(3)中红棕色变浅,2NO2?N2O4平衡右移,气体的总物质的量减少,压强减小,故D错误;
B、由于(3)中红棕色变浅,说明反应2NO2?N2O4向右移动,温度降低,所以NH4Cl溶于水时吸收热量,故B错误;
C、由于(1)中红棕色变深,平衡向着逆向移动,气体物质的量变大,混合气的相对分子质量减小,故C错误;
D、氧化钙溶于水放热,(1)中红棕色变深,说明反应2NO2?N2O4向左移动,该反应放热,故D正确;
故选D.
B、由于(3)中红棕色变浅,说明反应2NO2?N2O4向右移动,温度降低,所以NH4Cl溶于水时吸收热量,故B错误;
C、由于(1)中红棕色变深,平衡向着逆向移动,气体物质的量变大,混合气的相对分子质量减小,故C错误;
D、氧化钙溶于水放热,(1)中红棕色变深,说明反应2NO2?N2O4向左移动,该反应放热,故D正确;
故选D.
点评:本题考查了化学平衡移动的影响因素,注意根据反应的特点以及反应的现象判断平衡移动的方向,本题难度不大.

练习册系列答案
相关题目
如图所示,将锌片和铜片通过导线相连,置于稀硫酸中.下列说法正确的是( )
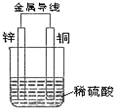

| A、铜片上有气泡逸出 |
| B、溶液的SO42-浓度逐渐减小 |
| C、电子由铜片经导线流向锌片 |
| D、该装置能将电能转化为化学能 |
下列实验结论或操作、生产方法,准确合理的是( )
| A、某钠盐溶于盐酸产生能使澄清石灰水变浑浊的无色无味气体,说明该钠盐是Na2CO3 |
| B、用饱和Na2CO3溶液除去CO2中混有的HCl |
| C、工业上常采用电解熔融MgO的方法制取金属镁 |
| D、除去MgCl2溶液中少量FeCl3可向其中加入足量Mg(OH)2粉末,充分搅拌后过滤 |
将a g甲醛(HCHO)、CH4和CO2的混合气体完全燃烧后,将燃烧后得到的混合气体被足量的Na2O2充分吸收,Na2O2的质量增重了a g,那么CH4与CO2的体积比为( )
| A、1:2 | B、1:1 |
| C、1:3 | D、任意比 |
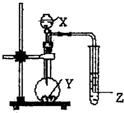 如图示的装置中,把X溶液逐滴滴下与Y物质反应,若X为浓硫酸,Y为第三周期金属元素中常温下与水难反应的单质.Z为品红溶液.实验中观察到Z褪色.则Y为( )
如图示的装置中,把X溶液逐滴滴下与Y物质反应,若X为浓硫酸,Y为第三周期金属元素中常温下与水难反应的单质.Z为品红溶液.实验中观察到Z褪色.则Y为( )| A、Na | B、Mg |
| C、Al | D、Mg或Al |
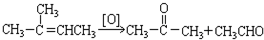
 在上述类似条件下发生反应,请写出反应的方程式:
在上述类似条件下发生反应,请写出反应的方程式: