题目内容
Ⅰ、(1)用NaOH配制0.1mol/L的NaOH溶液,应选用的仪器有 (选填序号).
a.烧瓶 b.容量瓶 c.量筒 d.胶头滴管
(2)电解法提纯工业生产中含有少量NO3-的aOH溶液,常用隔膜电解槽或离子膜电解槽.如图为阳离子交换膜电解槽(只允许阳离子通过)示意图.
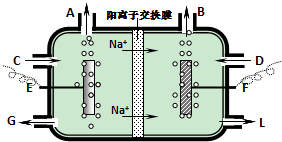
①请判断E为 极.
②B口处产生气体的化学式是 .
③制得的纯烧碱溶液从 处(填字母)流出.Ⅱ、有一瓶澄清的溶液,可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、Cl-和I-.取该溶液进行以下实验:
(1)取部分溶液,用pH试纸检验,溶液呈强酸性;
(2)取部分溶液,做焰色反应,透过蓝色钴玻璃发现火焰呈紫色;
(3)取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,溶液分层,下层呈紫红色;
(4)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
(5)取部分(4)得到的碱性溶液,加Na2CO3溶液,有白色沉淀生成;
(6)将(4)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝.
根据上述实验事实判断:在该溶液中肯定存在的离子是 ,肯定不存在的离子是 ,不能确定是否存在的离子是 .
a.烧瓶 b.容量瓶 c.量筒 d.胶头滴管
(2)电解法提纯工业生产中含有少量NO3-的aOH溶液,常用隔膜电解槽或离子膜电解槽.如图为阳离子交换膜电解槽(只允许阳离子通过)示意图.

①请判断E为
②B口处产生气体的化学式是
③制得的纯烧碱溶液从
(1)取部分溶液,用pH试纸检验,溶液呈强酸性;
(2)取部分溶液,做焰色反应,透过蓝色钴玻璃发现火焰呈紫色;
(3)取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,溶液分层,下层呈紫红色;
(4)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
(5)取部分(4)得到的碱性溶液,加Na2CO3溶液,有白色沉淀生成;
(6)将(4)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝.
根据上述实验事实判断:在该溶液中肯定存在的离子是
考点:配制一定物质的量浓度的溶液,常见离子的检验方法,电解原理
专题:基本概念与基本理论
分析:Ⅰ、(1)根据配制0.1mol/L的NaOH溶液的步骤选择使用的仪器;
(2)①根据电解槽中阳离子钠离子的移动方向判断电解池的阳极和阴极;
②根据电解原理判断B出通入的气体;
③根据电解原理判断制得的纯烧碱溶液流出位置;
Ⅱ、(1)溶液酸性强酸性,能够与氢离子反应的离子不能够存在;
(2)透过蓝色钴玻璃发现火焰呈紫色,说明一定存在钾离子;
(3)下层呈紫红色,溶液中存在碘单质;
(4)能够与氢氧化钠溶液反应生成难溶物的离子不能存在;
(5)生成沉淀为碳酸钡,溶液中存在偏铝酸根离子,说明原溶液中一定存在钡离子;
(6)能使湿润的红色石蕊试纸变蓝的气体是氨气,原溶液中一定存在铵离子.
(2)①根据电解槽中阳离子钠离子的移动方向判断电解池的阳极和阴极;
②根据电解原理判断B出通入的气体;
③根据电解原理判断制得的纯烧碱溶液流出位置;
Ⅱ、(1)溶液酸性强酸性,能够与氢离子反应的离子不能够存在;
(2)透过蓝色钴玻璃发现火焰呈紫色,说明一定存在钾离子;
(3)下层呈紫红色,溶液中存在碘单质;
(4)能够与氢氧化钠溶液反应生成难溶物的离子不能存在;
(5)生成沉淀为碳酸钡,溶液中存在偏铝酸根离子,说明原溶液中一定存在钡离子;
(6)能使湿润的红色石蕊试纸变蓝的气体是氨气,原溶液中一定存在铵离子.
解答:
解:Ⅰ、(1)配制0.1mol/L的NaOH溶液的步骤为:计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等,用到的仪器有托盘天平、烧杯、玻璃棒、胶头滴管、容量瓶等,所以b、d正确,
故答案为:b、d;
(2)①电解池中钠离子从E向F移动,外电路中电流方向为:F→E,外电路中电子移动方向与电流方向相反:E→F,所以电极E失去电子发生氧化反应,为电解池的阳极,F为阴极,
故答案为:阳极,
②电解氢氧化钠溶液,实质是电解水,阳极失去电子发生氧化反应生成氧气,阴极得到电子发生还原反应得到氢气,所以B产生的气体为氢气,
故答案为:H2,
③在电极F水中的氢离子得到电子生成氢气,溶液中产生了氢氧根离子,与钠离子形成氢氧化钠,所以制得的纯烧碱溶液从L流出,
故答案为:L;
Ⅱ、(1)取部分溶液,用pH试纸检验,溶液呈强酸性,溶液中一定不会存在CO32-;
(2)取部分溶液,做焰色反应,透过蓝色钴玻璃发现火焰呈紫色,说明溶液中一定存在K+;
(3)取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,溶液分层,下层呈紫红色,四氯化碳中溶有碘单质,原溶液中一定存在I-,因而一定不会存在Fe3+;
(4)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成,证明原溶液中一定不会存在:Mg2+、Al3+、Fe3+;
(5)取部分(4)得到的碱性溶液,加Na2CO3溶液,有白色沉淀生成,证明一定存在Ba2+,一定不会存在与钡离子反应生成硫酸钡沉淀的CO32-、SO42-;
(6)将(4)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,生成的气体为氨气,证明原溶液中一定存在NH4+;
所以一定存在的离子为:K+、NH4+、Ba2+、I-;一定不存在的离子为:Mg2+、Al3+、Fe3+、SO42-、CO32-;不能确定的离子为:Cl-,
故答案为:K+、NH4+、Ba2+、I-; Mg2+、Al3+、Fe3+、SO42-、CO32-;Cl-.
故答案为:b、d;
(2)①电解池中钠离子从E向F移动,外电路中电流方向为:F→E,外电路中电子移动方向与电流方向相反:E→F,所以电极E失去电子发生氧化反应,为电解池的阳极,F为阴极,
故答案为:阳极,
②电解氢氧化钠溶液,实质是电解水,阳极失去电子发生氧化反应生成氧气,阴极得到电子发生还原反应得到氢气,所以B产生的气体为氢气,
故答案为:H2,
③在电极F水中的氢离子得到电子生成氢气,溶液中产生了氢氧根离子,与钠离子形成氢氧化钠,所以制得的纯烧碱溶液从L流出,
故答案为:L;
Ⅱ、(1)取部分溶液,用pH试纸检验,溶液呈强酸性,溶液中一定不会存在CO32-;
(2)取部分溶液,做焰色反应,透过蓝色钴玻璃发现火焰呈紫色,说明溶液中一定存在K+;
(3)取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,溶液分层,下层呈紫红色,四氯化碳中溶有碘单质,原溶液中一定存在I-,因而一定不会存在Fe3+;
(4)另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成,证明原溶液中一定不会存在:Mg2+、Al3+、Fe3+;
(5)取部分(4)得到的碱性溶液,加Na2CO3溶液,有白色沉淀生成,证明一定存在Ba2+,一定不会存在与钡离子反应生成硫酸钡沉淀的CO32-、SO42-;
(6)将(4)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,生成的气体为氨气,证明原溶液中一定存在NH4+;
所以一定存在的离子为:K+、NH4+、Ba2+、I-;一定不存在的离子为:Mg2+、Al3+、Fe3+、SO42-、CO32-;不能确定的离子为:Cl-,
故答案为:K+、NH4+、Ba2+、I-; Mg2+、Al3+、Fe3+、SO42-、CO32-;Cl-.
点评:本题考查了配制一定物质的量浓度的溶液的仪器选择、常见的离子检验方法、电解原理等知识,题目难度中等,涉及的题量稍大,充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
设阿伏加德罗常数为NA,下列说法正确的是( )
| A、用100ml 4mol/L盐酸与8.7gMnO2共热能制取氯气0.2NA |
| B、一定温度下0.1L 0.1mol/L的HA和1L0.01mol/L的HA所含A-微粒数均为0.01NA |
| C、4.5 gSiO2晶体中含有的硅氧键数目为0.3 NA |
| D、标准状况下3.36 L CCl4含碳原子数为0.15NA |
物质的量相同的钠、镁、铝分别和足量稀硫酸反应,所产生气体的量是( )
| A、钠最多 | B、铝最少 |
| C、铝最多 | D、三者一样多 |
下列反应进行分类时,既属于氧化还原反应又属于化合反应的是( )
| A、Zn+H2SO4=ZnSO4+H2↑ | ||||
B、2KClO3
| ||||
C、S+O2
| ||||
D、CH4+2O2
|
下列关于有机物的叙述错误的是( )
| A、石油气、煤油和石蜡的主要成分都是碳氢化合物 |
| B、氯乙烷在NaOH水溶液中加热得到乙醇 |
C、由CH2=CH-COOCH3合成的聚合物为 |
| D、能与NaOH溶液反应且分子式为C2H4O2的有机物不一定是羧酸 |