题目内容
6.在下列有机物分子中,所有原子不可能处于同一平面的是( )| A. | CH2=CH-CN | B. | CH2=CH-CH=CH2 | C. | 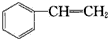 | D. | 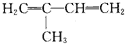 |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行判断.
解答 解:A.CH2=CHCN相当于乙烯分子中的一个氢原子被-CN取代,不改变原来的平面结构,-C≡N中两个原子在同一直线上,这两个平面可以是一个平面,所以该分子中所有原子可能在同一平面上,故A错误;
B.CH2=CH-CH=CH2相当于乙烯分子中的一个氢原子被乙烯基取代,不改变原来的平面结构,乙烯基的所有原子在同一个面上,这两个平面可以是一个平面,所以所有原子可能都处在同一平面上,故B错误;
C.苯为平面结构,苯乙烯相当于苯环上的一个氢被乙烯基取代,不改变原来的平面结构,乙烯基的所有原子在同一个面上,这两个平面可以是一个平面,所以所有原子可能都处在同一平面上,故C错误;
D.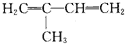 中含有甲基,甲基和甲烷具有相似的结构为空间四面体,所以所有原子不可能都处在同一平面上,故D正确;
中含有甲基,甲基和甲烷具有相似的结构为空间四面体,所以所有原子不可能都处在同一平面上,故D正确;
故选D.
点评 本题考查了学生对有机物的共面知识的认识,难度较大,分析时可根据已学过的甲烷、乙烯、苯的结构来类比判断.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
16.下列有关现在的长式元素周期表的判断中正确的是( )
| A. | 从左向右数第七纵行是ⅦA族 | |
| B. | 从左向右数第十一纵行是ⅠB族 | |
| C. | ⅠA族全部是金属元素 | |
| D. | 第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
17.将40℃的饱和NH4Cl溶液冷却至10℃,有NH4Cl固体析出.该过程中保持不变的是( )
| A. | 溶剂的质量 | B. | 溶质的质量分数 | ||
| C. | NH4Cl的溶解度 | D. | 溶液中NH4+的数目 |
14.某原电池的总反应离子方程式为2Fe3++Fe═3Fe2+,不能实现该反应的原电池是( )
| A. | 正极为Fe、负极为Fe,电解质溶液为FeCl3溶液 | |
| B. | 正极为Ag、负极为Fe,电解质溶液为CuSO4溶液 | |
| C. | 正极为Fe、负极为Zn,电解质溶液为Fe2(SO4)3溶液 | |
| D. | 正极为C、负极为Fe,电解质溶液为Fe(NO3)3溶液 |
1.A和B是前三周期的两种元素,它们的离子A2-和B3+具有相同的核外电子层结构.下列说法中正确的是( )
| A. | 原子半径:A>B | B. | 原子序数:B>A | ||
| C. | 元素所在周期序数:A>B | D. | 离子半径:B>A |
11.下列说法正确的是( )
| A. | 吸热反应一定是非自发的化学反应,放热反应不需要加热就能发生反应 | |
| B. | 其它条件不变时,增大压强可以增大活化分子百分数,使化学反应速率加快 | |
| C. | 温度、压强一定时,熵增加的反应都能自发进行 | |
| D. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 |
18.在25°C时,在水中通入氯化氢气体,当溶液的PH=3时,此时由水电离出的c(H+)是( )
| A. | 10-3mol/L | B. | 10-7 mol/L | C. | 10-11 mol/L | D. | 10-14mol/L |
15.下列说法中,正确的是( )
| A. | 强电解质溶液的导电能力一定比弱电解质强 | |
| B. | 冰醋酸是弱电解质,但液态时不能导电 | |
| C. | 盐酸中加入固体NaCl,因Cl-浓度增大,所以溶液酸性减弱 | |
| D. | 硫酸钠是强电解质,硫酸钡是弱电解质 |
16.下列叙述正确的是( )
| A. | 同周期元素的原子半径以ⅦA族的最大 | |
| B. | 同主族两种元素原子的核外电子数的差值可能为36 | |
| C. | 短周期中次外层电子数是最外层电子数2倍的原子一定是非金属元素的原子 | |
| D. | 科学家在周期表中金属与非金属分界线处找到了优良的催化剂 |