题目内容
如果1g水中含有a个氧原子,则阿伏加德罗常数是( )
| A、a mol-1 |
| B、18a mol-1 |
| C、2a mol-1 |
| D、9a mol-1 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:依据阿伏加德罗常数的含义进行计算,利用题给物理量用质量求的原子物质的量与用微粒数计算的物质的量相同.
解答:
解:阿伏伽德罗常数用NA表示,1g水的物质的量=
,含氧原子物质的量=
mol,a个氧原子物质的量=
mol,依据氧原子物质的量相同得到
=
mol,得到NA=18a/mol.
故选:B.
| 1g |
| 18g/mol |
| 1 |
| 18 |
| a |
| NA |
| 1 |
| 18 |
| a |
| NA |
故选:B.
点评:本题考查了阿伏加德罗常数的应用,质量、微粒数与物质的量的计算关系.

练习册系列答案
相关题目
下列所示的实验装置中,能达到实验目的是( )
A、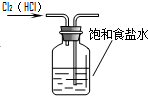 除去Cl2中的HCl |
B、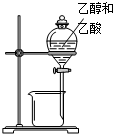 分离乙醇和乙酸 |
C、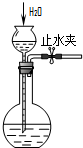 检查装置气密性 |
D、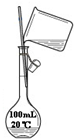 配制150 mL 0.10 mol?L-1盐酸 |
国际无机化学命名委员会将元素周期表原先的主、副族族号取消,从左往右改为18列第IA族为第1列,0族元素为第18列,按这个规定,下列说法不正确的是( )
| A、原子最外层有2个电子的元素,不一定是第2列元素 |
| B、第3~12列元素全为金属 |
| C、第17列元素的原子,其半径越大,越容易失去电子 |
| D、每列元素的单质,从上到下,熔沸点均依次增大 |
已知5KCl+KClO3+H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法正确的是( )
| A、KClO3是氧化剂,发生氧化反应 |
| B、氧化产物与还原产物质量比为5:1 |
| C、标准状况下,氯气的摩尔体积为22.4L |
| D、1mol KClO3参加反应时有10mol电子转移 |
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、在标准状况下,2.24L SO3(常温下为固体)中所含分子数为0.1NA |
| B、32g氧气和32g臭氧所含原子数均为2NA |
| C、在常温常压下,2.24L NH3所含质子数为10NA |
| D、1mol CO2和1mol CO均含有NA个分子,则所占体积也相同 |
下列溶液:①CH3COOH ②HCl ③NaOH ④CH3COONa ⑤KCl ⑥NH4Cl其物质的量浓度均为0.1mol/L,其pH由小到大排列顺序为( )
| A、③④⑤⑥①② |
| B、④⑤⑥①③② |
| C、②①⑥⑤④③ |
| D、②③①⑥⑤④ |
下列溶液中C(Cl-)与50mL 2mol?L-1 MgCl2溶液中C(Cl-)相等的是( )
| A、150 mL 2mol?L-1的NaCl溶液 |
| B、75mL 1mol?L-1的CaCl2溶液 |
| C、200mL 4mol?L-1的KCl溶液 |
| D、50 mL 1mol?L-1的AlCl3溶液 |
下列化学实验操作或事故处理方法正确的是( )
| A、实验做完后,直接用嘴吹灭酒精灯 |
| B、浓硫酸沾到皮肤上时,立即用湿抹布冲洗,然后涂上3%~5%的NaOH溶液 |
| C、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸 |
 A、B、C、D四种短周期元素,且A、D、B为相邻的同周期元素,C、B同主族,B、C可形成共价化合物BC3和BC2,A的原子结构示意图为如图,据此填空:
A、B、C、D四种短周期元素,且A、D、B为相邻的同周期元素,C、B同主族,B、C可形成共价化合物BC3和BC2,A的原子结构示意图为如图,据此填空: