题目内容
实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5L,回答下列问题.
(1)配制时,一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移⑥洗涤 ⑦定容 ⑧冷却.其正确的操作顺序为 .
(2)实验两次用到玻璃棒,其作用依次是: 、 .
(3)所需仪器为:量筒、容量瓶 (规格: )、托盘天平、药匙,还需要那些实验仪器才能完成该实验,请写出: 、 、 .
(4)试分析下列操作对所配溶液的浓度有何影响.
①为加速固体溶解,可稍微加热并不断搅拌.在未降至室温时,立即将溶液转移至溶量瓶定容.对所配溶液浓度的影响: .(填偏大、偏小、不变)
②定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度.对所配溶液浓度的影响 .(填偏大、偏小、不变)
③定容时俯视容量瓶刻度线,对所配溶液浓度的影响: .(填偏大、偏小、不变)
(1)配制时,一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移⑥洗涤 ⑦定容 ⑧冷却.其正确的操作顺序为
(2)实验两次用到玻璃棒,其作用依次是:
(3)所需仪器为:量筒、容量瓶 (规格:
(4)试分析下列操作对所配溶液的浓度有何影响.
①为加速固体溶解,可稍微加热并不断搅拌.在未降至室温时,立即将溶液转移至溶量瓶定容.对所配溶液浓度的影响:
②定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度.对所配溶液浓度的影响
③定容时俯视容量瓶刻度线,对所配溶液浓度的影响:
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据实验操作的步骤对各操作进行排序;
(2)根据玻璃棒有搅拌和引流作用来解答;
(3)根据配制一定物质的量浓度的步骤选择使用的仪器;
(4)根据c=
计算不当操作对n或V的影响,如果n偏大或V偏小,则所配制溶液浓度偏高,如果n偏小或V偏大,则配制浓度偏低,若n、v无变化,则配制浓度无影响.
(2)根据玻璃棒有搅拌和引流作用来解答;
(3)根据配制一定物质的量浓度的步骤选择使用的仪器;
(4)根据c=
| n |
| V |
解答:
解:(1)操作步骤有计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等操作,先计算,然后用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以操作顺序为②①③⑧⑤⑥④⑦④,
故答案为:②①③⑧⑤⑥④⑦④;
(2)玻璃棒在溶解时起到搅拌、加速溶解的作用,在移液时起到引流的作用,故答案为:搅拌,加速溶解;引流;
(3)配制500mL 1mol?L-1 NaCl溶液,需要的步骤有:计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等,由于容量瓶只有一条刻度线,故必须选用500ml容量瓶;需要使用的仪器有:托盘天平、药匙、烧杯、玻璃棒、量筒、500mL容量瓶、胶头滴管,
故答案为:500;烧杯;玻璃棒;胶头滴管;
(4)①溶液未降至室温时,立即将溶液转移至溶量瓶定容,待冷却后,液面会低于刻度线,即溶液体积偏小,则所配溶液的浓度偏大,故答案为:偏大;
②定容后,加盖倒转摇匀后,发现溶面低于刻度线是正常的,又滴加蒸馏水至刻度线,则所配溶液浓度的影响偏小,故答案为:偏小;
③定容时俯视容量瓶刻度线,溶液体积偏小,则所配溶液浓度偏大,故答案为:偏大.
故答案为:②①③⑧⑤⑥④⑦④;
(2)玻璃棒在溶解时起到搅拌、加速溶解的作用,在移液时起到引流的作用,故答案为:搅拌,加速溶解;引流;
(3)配制500mL 1mol?L-1 NaCl溶液,需要的步骤有:计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等,由于容量瓶只有一条刻度线,故必须选用500ml容量瓶;需要使用的仪器有:托盘天平、药匙、烧杯、玻璃棒、量筒、500mL容量瓶、胶头滴管,
故答案为:500;烧杯;玻璃棒;胶头滴管;
(4)①溶液未降至室温时,立即将溶液转移至溶量瓶定容,待冷却后,液面会低于刻度线,即溶液体积偏小,则所配溶液的浓度偏大,故答案为:偏大;
②定容后,加盖倒转摇匀后,发现溶面低于刻度线是正常的,又滴加蒸馏水至刻度线,则所配溶液浓度的影响偏小,故答案为:偏小;
③定容时俯视容量瓶刻度线,溶液体积偏小,则所配溶液浓度偏大,故答案为:偏大.
点评:本题考查配制一定物质的量浓度的溶液的操作顺序和仪器的选择、误差分析,题目难度中等,注意根据c=
计算不当操作对n或V的影响.
| n |
| V |

练习册系列答案
相关题目
下列各有机物的分类或命名正确的是( )
A、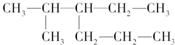 2甲基3丙基戊烷 2甲基3丙基戊烷 |
B、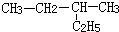 2-乙基丁烷 2-乙基丁烷 |
C、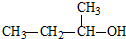 2-甲基-1-丙醇 2-甲基-1-丙醇 |
D、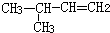 3-甲基-1-丁烯 3-甲基-1-丁烯 |