题目内容
19.有关钴和铁化合物的性质见下表.用含钴废料(含少量铁)可制备氯化钴:Co+2HCl═CoCl2+H2↑,工艺流程如下,试回答: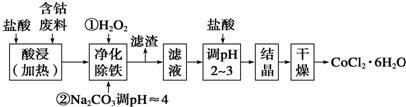
| 物质 | 溶度积Ksp | 沉淀完全时的pH |
| Co(OH)2 | 5.9×10-15 | 9.4 |
| Fe(OH)2 | 1.6×10-14 | 9.6 |
| Fe(OH)3 | 1.1×10-36 | 3.7 |
(2)生铁中含有一种铁碳化合物X(Fe3C).X在足量的空气中高温煅烧,生成有磁性的固体Y,Y可溶于过量盐酸,形成黄绿色的溶液,写出Y与盐酸反应的化学方程式Fe3O4+8HCl=2FeCl3+FeCl2+4H2O.
(3)“净化除铁”中,写出加入H2O2时反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(4)滤液的主要成分是CoCl2、NaCl、HCl.
(5)②步中用Na2CO3调pH≈4的原因是碳酸钠可与盐酸反应,降低溶液的酸性,增大pH,使铁离子沉淀完全.
分析 含钴废料(含少量铁)加入盐酸,可得CoCl2、FeCl2,加入过氧化氢,可得到FeCl3,然后加入Na2CO3调pH至4,可得到Fe(OH)3沉淀,过滤后所得滤液主要含有CoCl2、NaCl、HCl,为得到CoCl2•6H2O晶体,防止钴离子水解,加盐酸调节pH值在2~3,然后结晶、干燥得氯化钴晶体,
(1)钢铁在潮湿的空气中发生吸氧腐蚀,正极为氧气得电子生成氢氧根离子;
(2)Fe3C在足量的空气中高温煅烧,生成有磁性的固体Y应为四氧化三铁,四氧化三铁可溶于过量盐酸,生成氯化铁和氯化亚铁;
(3)双氧水具有氧化性,可以将亚铁离子氧化为正三价;
(4)当除尽Fe3+后,滤液中所含溶质有NaCl、CoCl2;
(5)根据Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-),pH=-lgc(H+),可知,pH>4Fe(OH)3沉淀完全;
解答 解:(1)钢铁在潮湿的空气中发生吸氧腐蚀,正极为氧气得电子生成氢氧根离子,电极反应式为O2+4e-+2H2O=4OH-,
故答案为:O2+4e-+2H2O=4OH-;
(2)Fe3C在足量的空气中高温煅烧,生成有磁性的固体Y应为四氧化三铁,四氧化三铁可溶于过量盐酸,生成氯化铁和氯化亚铁,反应的化学方程式为Fe3O4+8HCl=2FeCl3+FeCl2+4H2O,
故答案为:Fe3O4+8HCl=2FeCl3+FeCl2+4H2O;
(3)双氧水具有氧化性,可以将亚铁离子氧化为正三价,发生的化学反应为:2Fe2++H2O2+2H+=2Fe3++2H2O,
故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(4)除去Fe3+,滤液中主要含有NaCl、CoCl2、以及极少量的HCl,
故答案为:CoCl2、NaCl、HCl;
(5)滤液中(Fe3+)≤1.0×10-5mol/L时,可视为Fe3+沉淀完全,Ksp[Fe(OH)3]=1.0×10-35=c(Fe3+)×c3(OH-)=1.0×10-5mol•L-1×c3(OH-),所以c(OH-)=10-10mol•L-1,c(H+)=$\frac{10{\;}^{-14}}{10{\;}^{-10}}$mol•L-1=10-4mol•L-1,PH=-lgc(H+)=-lg10-4=4,所以为了使Fe3+完全沉淀,用Na2CO3调pH≈4,碳酸钠可与盐酸反应,降低溶液的酸性,增大pH,使铁离子沉淀完全,
故答案为:碳酸钠可与盐酸反应,降低溶液的酸性,增大pH,使铁离子沉淀完全;
点评 本题综合考查物质的制备和提纯等知识,是一道综合性很强的实验探究题,侧重于学生的分析能力、实验能力和计算能力的考查,为高考常见题型,注意把握实验的操作原理和步骤,把握相关物质的性质,难度中等.

| A. | 用盐酸滴定氢氧化钠溶液时向锥形瓶中量取25.00mL的氢氧化钠溶液 | |
| B. | 用量筒测得排水法收集制得的氢气体积为50.28 mL | |
| C. | 用两只250 mL的容量瓶配制0.1 mol•L-1 500 mL的NaOH溶液 | |
| D. | 用托盘天平称取2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g |
| A. | 充电时阳极反应:NiOOH+H2O+e-═Ni(OH)2+OH- | |
| B. | 充电过程是电能转化为化学能的过程 | |
| C. | 放电时负极附近溶液的碱性不变 | |
| D. | 放电时电解质溶液中的OH-向正极移动 |
| A. | LiOH | B. | KOH | C. | RbOH | D. | NaOH |
| A. | 金属甲比金属乙容易失去电子,则甲比乙金属性强 | |
| B. | NaHCO3与NaOH反应有CO2生成 | |
| C. | 稀硝酸能将亚铁离子氧化为铁离子 | |
| D. | Na2CO3不能用于治疗胃酸过多 |
| A. | pH=12的溶液中:AlO2-、Na+、SO42-、SO32- | |
| B. | 水电离出的c(H+)=1×10-12 mol•L-1的溶液中:K+、Na+、SO42-、AlO2- | |
| C. | 加入甲基橙呈黄色的溶液:NH4+、Fe2+、Cl-、NO3- | |
| D. | c(H+)=0.10 mol•L-1的溶液中:CH3COO-、NH4+、Cl-、Na+ |
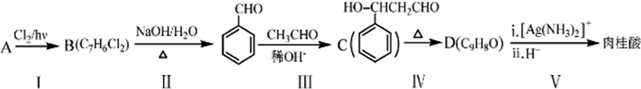

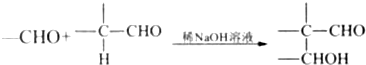
 .
. .肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是
.肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是 .
.