题目内容
11.下列叙述正确的是( )| A. | 汽油、柴油和地沟油都是碳氢化合物 | |
| B. | 石油的分馏和煤的干馏都是化学变化 | |
| C. | 苯环内含有碳碳单键和碳碳双键 | |
| D. | 纤维素、淀粉、蛋白质在一定条件下都能发生水解反应 |
分析 A.仅由碳和氢两种元素组成的有机化合物称为碳氢化合物;
B.石油的分馏是物理过程;
C.苯环内无碳碳单键和碳碳双键;
D.多糖可水解为二糖、单糖,蛋白质可水解为氨基酸;
解答 解:A.汽油、柴油都是碳氢化合物,地沟油的主要成分为油脂,油脂的成分是高级脂肪酸甘油酯,含碳、氢、氧三种元素,故A错误;
B.石油的分馏属于物理变化,煤的干馏属于化学变化,故B错误;
C.苯环内无碳碳单键和碳碳双键,是一种介于单键、双键之间的一种特殊的键,故C错误;
D.纤维素和淀粉属于多糖,多糖可水解为二糖、单糖,蛋白质可水解为氨基酸,故D正确;
故选:D.
点评 本题考查了石油的分馏和煤的干馏、多糖和蛋白质的水解、苯环的结构,题目难度不大,注意基础知识的积累.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
10.当航天飞机返回地球进入大气层时,由于空气的剧烈磨擦,航天飞机尖端的温度可达1000℃以上.为了防止极高的温度将其烧毁,科学家给航天飞机相应部位设计安装了可靠的保护层.制作保护层的材料可能为( )
| A. | 合成塑料 | B. | 合成纤维 | C. | 镁铝合金 | D. | 新型陶瓷 |
2.某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂.请填写下列空白:
(1)下列有关滴定操作的顺序正确的是B
①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液 ③检查滴定管是否漏水 ④滴定 ⑤洗涤
A.⑤①②③④B.③⑤①②④C.③⑤②①④D.②①③⑤④
(2)用标准的盐酸滴定待测的NaOH溶液时,一手握酸式滴定管的活塞,一手摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,本实验滴定达到终点的标志是溶液颜色由黄色突变为橙色,且半分钟内不变色
(3)下列哪些操作会使测定结果偏高ABC
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后未用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数仰视滴定管读数,滴定后俯视滴定管读数
(4)某学生根据3次实验分别记录有关数据如下表:
则该NaOH溶液的物质的量浓度为0.1112mol/L.
(1)下列有关滴定操作的顺序正确的是B
①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液 ③检查滴定管是否漏水 ④滴定 ⑤洗涤
A.⑤①②③④B.③⑤①②④C.③⑤②①④D.②①③⑤④
(2)用标准的盐酸滴定待测的NaOH溶液时,一手握酸式滴定管的活塞,一手摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,本实验滴定达到终点的标志是溶液颜色由黄色突变为橙色,且半分钟内不变色
(3)下列哪些操作会使测定结果偏高ABC
A.锥形瓶用蒸馏水洗净后再用待测液润洗
B.酸式滴定管用蒸馏水洗净后未用标准液润洗
C.滴定前酸式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数仰视滴定管读数,滴定后俯视滴定管读数
(4)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0mol•L-1盐酸的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 20.00 | 0.00 | 22.20 |
| 第二次 | 20.00 | 1.56 | 25.50 |
| 第三次 | 20.00 | 0.22 | 22.48 |
19.下列各组气体,在通常条件下能稳定共存的是( )
| A. | NH3、O2、HCl | B. | N2、H2、HCl | C. | CO2、NO、O2 | D. | H2S、O2、SO2 |
6.请回答下列问题:
(1)N、Al、Si、Zn、Fe五种元素中,有一种元素的电离能数据如下:
则该元素是Al(填写元素符号).N原子的价电子排布图为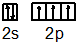 .
.
(2)已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+,1mol该离子含有σ键的数目为15NA;
(3)K3[Fe(CN)6]可用来检验Fe2+,向硫酸亚铁溶液中加入几滴K3[Fe(CN)6],观察到的现象是产生蓝色沉淀,与CN-互为等电子体的微粒有CO、N2等(填化学式,写2种)
C、N、O三种元素第一电离能由大到小的顺序为N>O>C;三种元素形成的简单氢化物分子中键角由大到小依次为CH4>NH3>H2O(用分子式表示).
(4)已知Fe的相对原子质量为M,阿佛加德罗常数用NA表示,已知金属Fe为体心立方堆积,若Fe原子半径为acm,密度为ρg/cm3.则M=$\frac{32ρ{a}^{3}{N}_{A}}{3\sqrt{3}}$(用ρ、a、NA表达式表示)
(1)N、Al、Si、Zn、Fe五种元素中,有一种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | … |
| Im/kJ•mol-1 | 578 | 1817 | 2745 | 11578 | … |
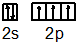 .
.(2)已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+,1mol该离子含有σ键的数目为15NA;
(3)K3[Fe(CN)6]可用来检验Fe2+,向硫酸亚铁溶液中加入几滴K3[Fe(CN)6],观察到的现象是产生蓝色沉淀,与CN-互为等电子体的微粒有CO、N2等(填化学式,写2种)
C、N、O三种元素第一电离能由大到小的顺序为N>O>C;三种元素形成的简单氢化物分子中键角由大到小依次为CH4>NH3>H2O(用分子式表示).
(4)已知Fe的相对原子质量为M,阿佛加德罗常数用NA表示,已知金属Fe为体心立方堆积,若Fe原子半径为acm,密度为ρg/cm3.则M=$\frac{32ρ{a}^{3}{N}_{A}}{3\sqrt{3}}$(用ρ、a、NA表达式表示)
16.如表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断下列叙述不正确的是( )
| 元素代号 | A | B | C | D | E | F | G |
| 原子半径/nm | 0.182 | 0.160 | 0.089 | 0.143 | 0.102 | 0.099 | 0.071 |
| 主要化合价 | +1 | +2 | +2 | +3 | +6.-2 | -1 | -1 |
| A. | 气态氢化物的稳定性HG>HF>H2E | |
| B. | B2+、D3+、E2-、G-四种离子的核外电子排布相同 | |
| C. | A、E元素与氧元素可以形成三种常见的含氧酸盐 | |
| D. | F、G元素的氢化物沸点G>F |
1.金属铝可以溶于氢氧化钠溶液,有关该反应,下列说法正确的是( )
| A. | 同时生成的气体是氧气 | |
| B. | 氧化剂是氢氧化钠和水 | |
| C. | 当产生1.5mol气体时电子转移3NA个 | |
| D. | 这个反应体现了金属的通性 |