题目内容
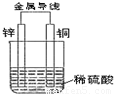
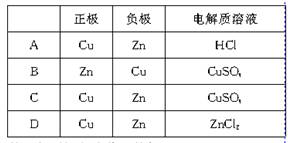
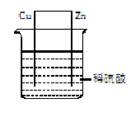
关于如图组成的原电池的说法中,正确的是( )
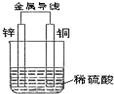

分析:锌比铜活泼,应为原电池的负极,发生氧化反应,电极方程式为Zn-2e-=Zn2+,铜为原电池的正极,发生还原反应,电极方程式为2H++2e-=H2↑,以此解答该题.
解答:解:A.铁比铜活泼,柠檬溶液呈酸性,将铜丝和铁丝连接插在柠檬中可形成原电池,故A正确;
B.锌比铜活泼,应为原电池的负极,发生氧化反应,故B错误;
C.铜电极反应为2H++2e-=H2↑,有气泡生成,故C错误;
D.原电池工作时,电流由铜片经外电路流向锌片,即由正极流向负极,故D错误.
故选A.
B.锌比铜活泼,应为原电池的负极,发生氧化反应,故B错误;
C.铜电极反应为2H++2e-=H2↑,有气泡生成,故C错误;
D.原电池工作时,电流由铜片经外电路流向锌片,即由正极流向负极,故D错误.
故选A.
点评:本题考查原电池知识,侧重于原电池的组成和原理的考查,题目难度不大,注意原电池的正负极的判断以及原电池的工作原理的把握.

练习册系列答案
相关题目