题目内容
在一定温度下,当Mg(OH)2固体在水溶液中达到下列平衡时:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),若使固体Mg(OH)2的量减少,而且c(Mg2+)不变,可采取的措施是( )
| A、加MgCl2 |
| B、加H2O |
| C、加NaOH |
| D、加HCl |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:要使Mg(OH)2固体减少,应使平衡向正向移动,但c(Mg2+)不变,说明仍为饱和溶液,可加入水,以此解答该题.
解答:
解:A.加入固体MgCl2,增大了c(Mg2+),使溶解平衡逆向移动,悬浊液中Mg(OH)2固体的质量增加,故A错误;
B.加入适量水,使溶解平衡正向移动,悬浊液中Mg(OH)2固体的质量减少,由于加水后仍是Mg(OH)2的饱和溶液,所以c(Mg2+)不变,故B正确;
C.加入NaOH固体,增大了c(OH-),使溶解平衡逆向移动,悬浊液中Mg(OH)2固体的质量增加,c(Mg2+)减小,故C错误;
D.加适量盐酸,消耗了氢氧根离子,使溶解平衡正向移动,悬浊液中Mg(OH)2固体的质量减少,c(Mg2+)增加,故D错误;
故选:B.
B.加入适量水,使溶解平衡正向移动,悬浊液中Mg(OH)2固体的质量减少,由于加水后仍是Mg(OH)2的饱和溶液,所以c(Mg2+)不变,故B正确;
C.加入NaOH固体,增大了c(OH-),使溶解平衡逆向移动,悬浊液中Mg(OH)2固体的质量增加,c(Mg2+)减小,故C错误;
D.加适量盐酸,消耗了氢氧根离子,使溶解平衡正向移动,悬浊液中Mg(OH)2固体的质量减少,c(Mg2+)增加,故D错误;
故选:B.
点评:本题考查难溶电解质的溶解平衡和沉淀的转化,为高频考点,侧重于学生的分析能力的考查,题目难度不大,注意从平衡移动的角度解答该题.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
有关化学资源的合成、利用与开发的叙述合理的是( )
| A、大量使用化肥和农药,能不断提高农作物产量 |
| B、通过有机合成,可以制造出比钢铁更强韧的新型材料 |
| C、安装煤炭燃烧过程的“固硫”装置,主要是为了提高煤的利用率 |
| D、开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理 |
分子式为C7H8O的芳香化合物中,与FeCl3溶液混合显紫色和不显紫色的物质分别有( )
| A、2种和1种 |
| B、2种和3种 |
| C、3种和2种 |
| D、3种和1种 |
关于0.1mol?L-1 NaHCO3溶液,下列说法正确的是( )
| A、溶质水解反应:HCO3-+H2?H3O++CO32- |
| B、离子浓度关系:c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) |
| C、微粒浓度关系:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-) |
| D、微粒浓度关系:c(Na+)═2[c(H2CO3)+c(HCO3-)+c(CO32-)] |
如图为雾霾的主要成分示意图.下列说法不正确的是( )
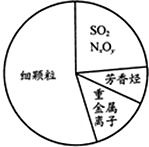

| A、重金属离子可导致蛋白质变性 |
| B、苯是最简单的芳香烃 |
| C、SO2和NxOy都属于酸性氧化物 |
| D、汽车尾气的大量排放是造成雾霾天气的人为因素之一 |
下列物质之间反应,不可能发生爆炸的是( )
| A、H2与F2 |
| B、H2与I2 |
| C、H2与O2 |
| D、Na与S |
下列说法正确的是( )
| A、弱碱溶于水后能促进水的电离 |
| B、盐溶于水后一定能促进水的电离 |
| C、任何条件下,只要pH>7,溶液就一定显碱性 |
| D、任何条件下,只要c(H+)>c(OH-),溶液就一定显酸性 |
下列有关化学用语正确的是( )
A、Cl-离子的结构示意图: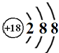 |
B、次氯酸的电子式 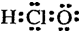 |
C、丙烷分子的比例模型示意图: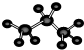 |
D、甲烷的结构式为: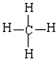 |
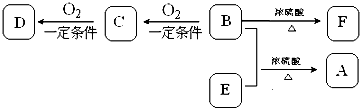
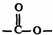 基团:
基团: