题目内容
3.有FeO、Fe2O3的混合物若干克,在足量H2气流中加热充分反应,冷却后称得剩余固体比原混合物减轻0.8g;将等质量的原混合物与盐酸反应,欲使之完全溶解,至少需要1mol/L盐酸的体积为( )| A. | 0.1L | B. | 0.2L | C. | 0.5L | D. | 1.0L |
分析 在H2气流中加热充分反应,冷却后称剩余固体比原混合物质量减轻0.8g,减少的质量为O元素的质量,将FeO、Fe2O3的混合物与盐酸反应生成FeCl2、FeCl3的混合物,相当于其中的O被Cl代替,根据化合价守恒计算盐酸的体积,1个O被2个Cl代替.
解答 解:FeO、Fe2O3的混合物若干克,在H2气流中加热充分反应,生成Fe,冷却后称剩余固体比原混合物质量减轻0.8g,则减少的质量为O元素的质量,将FeO、Fe2O3的混合物与盐酸反应生成FeCl2、FeCl3的混合物,相当于其中的O被Cl代替,根据化合价守恒,1个O被2个Cl代替.所以需1 mol•L-1的盐酸的体积 V(HCl)=$\frac{\frac{0.8g}{16g/mol}×2}{1mol/L}$=0.1L,
故选A.
点评 本题考查混合物反应的计算,题目难度中等,本题计算时可从化合物组成的角度分析,从化合价守恒的角度解答,可以省去过程的繁琐.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下述实验设计能够达到目的是( )
| 编号 | 实验目的 | 实验设计 |
| A | 除去CO2中少量的SO2 | 将混合气体通过饱和Na2CO3溶液 |
| B | 除去Cu粉中混有的CuO | 向混合物中滴加适量稀硝酸 |
| C | 证明H2CO3酸性比苯酚强 | 将CO2通入苯酚钠溶液中 |
| D | 检验溶液中是否含有Fe2+ | 向溶液中滴入氯水水后,再滴加KSCN 溶液 |
| A. | A | B. | B | C. | C | D. | D |
11.下列实验操作和所用玻璃仪器都正确的是( )
| 选项 | 实验操作 | 玻璃仪器 |
| A | 分离苯和NaOH溶液 | 分液漏斗、烧杯 |
| B | 用直接蒸馏的方法分离乙醇和乙酸 | 蒸馏烧瓶、冷凝管、锥形瓶 |
| C | 配制100mL pH=1的CH3COOH溶液 | 1 00mL容量瓶、胶头滴管、烧杯、玻璃棒、量筒 |
| D | 利用MnO2和浓盐酸制备并收集Cl2 | 酒精灯、烧杯、导管、集气瓶 |
| A. | A | B. | B | C. | C | D. | D |
18.与50mL0.5mol/L的(NH4)2SO4溶液中,c(NH4+)浓度相同的是( )
| A. | 100mL1mol/L的氨水 | B. | 200mL1mol/L的NH4Cl | ||
| C. | 50mL0.5mol/L的CH3COONH4溶液 | D. | 50mL0.5mol/L的NH4NO3 |
8.下列关于有机物性质的说法正确的是( )
| A. | 乙烯可以与氯气反应甲烷不能 | |
| B. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 | |
| C. | 乙烯和苯都能使酸性高锰酸钾溶液褪色 | |
| D. | 乙烯和乙烷都可以发生氧化反应 |
15.下列离子方程式正确的是( )
| A. | 硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ | |
| B. | 将大理石投入到足量盐酸中:CO32-+2H+═CO2↑+H2O | |
| C. | 将Cl2通入KI溶液中:2I-+Cl2═2Cl-+I2 | |
| D. | 碳酸钠溶液显碱性:CO32-+H2O═HCO3-+OH- |
12.下列叙述中错误的是( )
| A. | ⅢA族的B元素和ⅦA族的F元素能形成离子化合物BF3 | |
| B. | Na+和O2-电子层结构相同,Na+比O2-半径小 | |
| C. | IA族元素中,原子半径最大的金属性最强 | |
| D. | 第3周期元素中,原子序数最大的非金属性最强 |
12.工业上可由乙苯生产苯乙烯: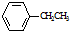 $→_{加热}^{Fe_{2}O_{2}}$
$→_{加热}^{Fe_{2}O_{2}}$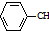 =CH2+H2,下列说法正确的是( )
=CH2+H2,下列说法正确的是( )
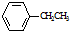 $→_{加热}^{Fe_{2}O_{2}}$
$→_{加热}^{Fe_{2}O_{2}}$ =CH2+H2,下列说法正确的是( )
=CH2+H2,下列说法正确的是( )| A. | 可用酸性高锰酸钾溶液鉴别乙苯和苯乙烯 | |
| B. | 乙苯、苯乙烯能使溴水褪色,原因是两者发生了氧化反应 | |
| C. | 该反应的反应类型为消去反应 | |
| D. | 乙苯和苯乙烯分子内共平面的碳原子数最多均为7 |