题目内容
 最近发现一种由某金属原子M和非金属原子N构成的气态团簇分子,如图所示.顶角和面心的原子是M原子,棱的中心和体心的原子是N原子,它的化学式为( )
最近发现一种由某金属原子M和非金属原子N构成的气态团簇分子,如图所示.顶角和面心的原子是M原子,棱的中心和体心的原子是N原子,它的化学式为( )| A、M4N4 |
| B、MN |
| C、M14N13 |
| D、M4N5 |
考点:晶胞的计算
专题:化学键与晶体结构
分析:仔细审题可知,所描述的物质是一分子,即MN原子并不存在共用关系.
解答:
解:由气态团簇分子和图可知其分子式可由示意图查原子个数来确定,M原子共14个,N原子13个,即分子式为M14N13,
故选C.
故选C.
点评:本题考查晶体类型,难度不大,但是容易出错,应该读懂题意,真正的领会题目意图.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
下列说法不正确的是( )
| A、二氯甲烷、溴已烷、盐酸甘氨酸都是共价化合物 |
| B、酚醛树脂、聚乙烯、天然橡胶都是由高分子化合物组成的物质 |
| C、有机物均含有C元素,但不是所有有机物均能发生燃烧反应 |
| D、水溶液的PH不同,氨基酸在水溶液中存在形式不同,可以调节PH分离氨基酸 |
下列说法正确的是( )
| A、pH=5的盐酸,再加水冲稀1000倍,溶液的pH=8 |
| B、给稀醋酸溶液加热,溶液pH值增大 |
| C、pH=1的盐酸中c(H+)是pH=3的盐酸的c(H+)100倍 |
| D、在H2CO3溶液中,C(H+):C(CO32-)=2:1 |
下列各项操作中,出现“先产生沉淀,然后沉淀又溶解”现象的是( )
①向饱和碳酸钠溶液中通入过量的CO2 ②向漂白粉溶液中缓慢通入过量的CO2
③向NaAlO2溶液中通入过量的CO2 ④向澄清石灰水中缓慢通入过量的SO2.
①向饱和碳酸钠溶液中通入过量的CO2 ②向漂白粉溶液中缓慢通入过量的CO2
③向NaAlO2溶液中通入过量的CO2 ④向澄清石灰水中缓慢通入过量的SO2.
| A、①② | B、②④ | C、①③ | D、②③ |
下列说法不正确的是( )
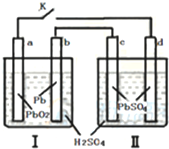

| A、我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流.电池总反应为:4Al+3O2+6H2O═4Al(OH)3,该电池通常只需更换铝板就可继续使用 | |||
B、铅蓄电池的工作原理为:Pb+PbO2+2H2SO4
| |||
| C、金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,(已知:氧化性Fe2+<Ni2+<Cu2+)电解后,电解槽底部的阳极泥中只有Cu和Pt | |||
| D、判断一种电池的优劣标准是:电池的成本 |
火法炼铜过程中发生如下反应:Cu2S+O2═2Cu+SO2.下列说法正确的是( )
| A、Cu2S是还原剂,O2是氧化剂 |
| B、Cu是还原产物,SO2是氧化产物 |
| C、1 mol Cu2S和O2反应生成2 mol Cu,转移电子数的物质的量为6 mol |
| D、反应消耗3 mol Cu2S时,被O2氧化的硫(S)的物质的量为3 mol |
将1.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,一定条件下发生反应:PCl3(g)+Cl2(g)?PCl5(g),达到平衡时PCl5为0.3mol?L-1,如果此时再充入1.0molPCl3和1.0mol Cl2,在相同温度下再达到平衡时,PCl5的物质的量浓度是( )
| A、0.6mol?L-1 |
| B、大于0.3 mol?L-1,小于0.6 mol?L-1 |
| C、大于0.6 mol?L-1 |
| D、小于0.3 mol?L-1 |

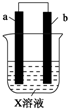 下列对如图所示装置实验判断的描述正确的是( )
下列对如图所示装置实验判断的描述正确的是( )