题目内容
1.某元素天然同位素原子A的一个原子中共有96个微粒,其中36个微粒不带电.则A的相对原子质量接近( )| A. | 36 | B. | 30 | C. | 66 | D. | 60 |
分析 A的一个原子中共有96个微粒,其中36个微粒不带电,可知中子数为36,质子数=核外电子数=$\frac{96-36}{2}$=30,原子的质量主要集中在原子核上,以此来解答.
解答 解:原子由质子、中子、电子构成,A的一个原子中共有96个微粒,其中36个微粒不带电,可知中子数为36,质子数=核外电子数=$\frac{96-36}{2}$=30,原子的质量主要集中在原子核上,则A的相对原子质量接近30+36=66,
故选C.
点评 本题考查物质的量的计算,为高频考点,把握原子的构成、质子数与中子数为解答的关键,侧重分析与计算能力的考查,注意原子的构成,题目难度不大.

练习册系列答案
相关题目
11.下列离子方程式书写正确的是( )
| A. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 氢氧化钡溶液与盐酸反应:OH-+H+═H2O | |
| D. | 硫酸铜溶液与氢氧化钡溶液混合:Cu2++2 OH-═Cu(OH)2↓ |
9. 将一定质量的Mg和Al的混合物投入2.0mol•L-1,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图示.则下列说法正确的是( )
将一定质量的Mg和Al的混合物投入2.0mol•L-1,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图示.则下列说法正确的是( )
 将一定质量的Mg和Al的混合物投入2.0mol•L-1,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图示.则下列说法正确的是( )
将一定质量的Mg和Al的混合物投入2.0mol•L-1,250mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图示.则下列说法正确的是( )| A. | 当加氢氧化钠溶液体积为20mL时,溶液的pH值等于7 | |
| B. | 当加氢氧化钠溶液体积为20mL时,溶液中的溶质只有硫酸镁和硫酸铝 | |
| C. | NaOH溶液的物质的量浓度为5 mol•L-1 | |
| D. | 生成的H2在标准状况下的体积为11.2L |
16.下列说法中,不正确的是( )
| A. | 1mol任何物质都含有6.02×1021个原子, | |
| B. | 0.012kg12C含有6.02×1023碳原子 | |
| C. | 阿伏伽德罗常数表示的粒子“集体”就是1mol | |
| D. | 使用摩尔这一单位时必须指明粒子的名称 |
9.碘在人体中含量极少,却对人体机能的正常运行起着十分重要的作用.儿童缺碘会导致( )
| A. | 多动症 | B. | 发育迟缓 | C. | 焦虑失眠 | D. | 甲状腺肿大 |
 .
.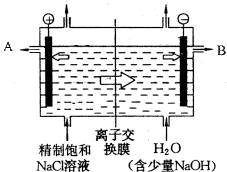 工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水.图为离子交换膜法电解原理示意图:
工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水.图为离子交换膜法电解原理示意图: