题目内容
欲配制 1mol/L Na2CO3 溶液250mL,完成下列步骤:
(1)用托盘天平称取 Na2CO3 固体______ g.
(2)将称好的Na2CO3固体放入______中加少量蒸馏水将其溶解,待______后,将溶液沿______移入______mL的容量瓶内.
(3)用少量蒸馏水冲洗______次,将冲洗液移入______中,在操作过程中不得损失点滴溶液,否则会使溶液的浓度偏______(高或低).
(4)向容量瓶内加水至距刻线______时,改用______小心加水至溶液凹液面与刻线相切,若加水超过刻线,会造成溶液偏______(低或高),应该______.
(5)最后盖好瓶塞______,将配好的溶液移入______并贴好标签.
解:(1)需Na2CO3的质量为m=0.25L×1mol?L-1×106g/mol=26.5g,故答案为:26.5g;
(2)将称好的Na2CO3固体放入烧杯中加少量蒸馏水将其溶解,待冷却至室温后,将溶液沿玻璃棒移入250ml的容量瓶内,
故答案为:烧杯;冷却至室温;玻璃棒;250;
(3)用少量蒸馏水冲洗 2~3次,将冲洗液移入容量瓶中;在操作过程中不得损失点滴溶液,导致a2CO3的质量减小,会使溶液的浓度偏低,
故答案为:2~3;容量瓶;低;
(4)向容量瓶内加水至距刻线 1~2cm时,改用胶头滴管小心加水至溶液凹液面与刻线相切;加水超过刻线,导致溶液体积增大,会造成溶液偏低,应该重新配制,
故答案为:1~2cm;胶头滴管;低;重新配制;
(5)最后盖好瓶塞颠倒摇匀,将配好的溶液移入试剂瓶并贴好标签,故答案为:颠倒摇匀;试剂瓶.
分析:(1)利用n=cv计算出Na2CO3的物质的量,再根据m=nM计算所需Na2CO3的质量;
(2)将称好的Na2CO3固体放入烧杯中加少量蒸馏水将其溶解,待冷却至室温后,将溶液沿玻璃棒移入250ml的容量瓶内;
(3)用少量蒸馏水冲洗 2~3次,将冲洗液移入容量瓶中;
分析操作对溶质的物质的量或对溶液的体积的影响,根据c=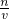 分析判断;
分析判断;
(4)向容量瓶内加水至距刻线 1~2cm时,改用胶头滴管小心加水至溶液凹液面与刻线相切;
分析操作对溶质的物质的量或对溶液的体积的影响,根据c=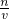 分析判断;
分析判断;
(5)最后盖好瓶塞颠倒摇匀,将配好的溶液移入试剂瓶并贴好标签.
点评:本题考查溶液的配制实验,题目难度不大,关键清楚溶液配制的原理,通过c=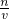 可以加深理解.注意实验的基本操作方法和注意事项.
可以加深理解.注意实验的基本操作方法和注意事项.
(2)将称好的Na2CO3固体放入烧杯中加少量蒸馏水将其溶解,待冷却至室温后,将溶液沿玻璃棒移入250ml的容量瓶内,
故答案为:烧杯;冷却至室温;玻璃棒;250;
(3)用少量蒸馏水冲洗 2~3次,将冲洗液移入容量瓶中;在操作过程中不得损失点滴溶液,导致a2CO3的质量减小,会使溶液的浓度偏低,
故答案为:2~3;容量瓶;低;
(4)向容量瓶内加水至距刻线 1~2cm时,改用胶头滴管小心加水至溶液凹液面与刻线相切;加水超过刻线,导致溶液体积增大,会造成溶液偏低,应该重新配制,
故答案为:1~2cm;胶头滴管;低;重新配制;
(5)最后盖好瓶塞颠倒摇匀,将配好的溶液移入试剂瓶并贴好标签,故答案为:颠倒摇匀;试剂瓶.
分析:(1)利用n=cv计算出Na2CO3的物质的量,再根据m=nM计算所需Na2CO3的质量;
(2)将称好的Na2CO3固体放入烧杯中加少量蒸馏水将其溶解,待冷却至室温后,将溶液沿玻璃棒移入250ml的容量瓶内;
(3)用少量蒸馏水冲洗 2~3次,将冲洗液移入容量瓶中;
分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
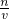 分析判断;
分析判断;(4)向容量瓶内加水至距刻线 1~2cm时,改用胶头滴管小心加水至溶液凹液面与刻线相切;
分析操作对溶质的物质的量或对溶液的体积的影响,根据c=
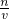 分析判断;
分析判断;(5)最后盖好瓶塞颠倒摇匀,将配好的溶液移入试剂瓶并贴好标签.
点评:本题考查溶液的配制实验,题目难度不大,关键清楚溶液配制的原理,通过c=
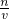 可以加深理解.注意实验的基本操作方法和注意事项.
可以加深理解.注意实验的基本操作方法和注意事项. 
练习册系列答案
相关题目