题目内容
3.下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )| A. | 氢氧化钠与盐酸; 氢氧化钠与碳酸 | |
| B. | BaCl2溶液与Na2SO4溶液; Ba(OH)2溶液与H2SO4溶液 | |
| C. | Na2CO3溶液与硝酸溶液; CaCO3溶液与硝酸溶液 | |
| D. | 石灰石与硝酸反应; 石灰石与盐酸 |
分析 A.盐酸为强酸,而碳酸为弱酸;
B.BaCl2溶液与Na2SO4溶液生成硫酸钡沉淀和氯化钠,Ba(OH)2溶液与H2SO4溶液生成硫酸钡和水;
C.碳酸钠为易溶性盐,碳酸钙为沉淀;
D.二者反应实质都是碳酸钙与氢离子反应生成钙离子和水、二氧化碳.
解答 解:A.盐酸为强酸,书写离子方程式应拆开,而碳酸为弱酸,应保留化学式,所以二者的离子反应不同,故A不选;
B.BaCl2溶液与Na2SO4溶液反应的离子反应为Ba2++SO42-═SO4↓,但Ba(OH)2溶液与H2SO4溶液除生成硫酸钡沉淀还生成水,则二者离子反应不同,故B不选;
C.碳酸钠为易溶性盐,书写离子方程式应拆开,碳酸钙为沉淀,应保留化学式,所以二者的离子反应不同,故C不选;
D.二者反应实质都是碳酸钙与氢离子反应生成钙离子和水、二氧化碳,都可以用离子方程式:CaCO3+2H+═Ca2++H2O+CO2↑表示,故D选;
故选:D.
点评 本题考查离子反应方程式,明确发生的离子反应是解答本题的关键,并熟悉离子反应方程式的书写方法来解答,难度不大.

练习册系列答案
相关题目
13.有一份溶液中只有K+、Na+、NO3-、CO32-四种离子大量存在,经测定,c(Na+)=2.0mol/L,c(K+)=2.5mol/L,c(CO32-)=1.8mol/L,则溶液中NO3-的物质的量浓度为( )
| A. | 2.7 mol/L | B. | 1.35 mol/L | C. | 0.9 mol/L | D. | 0.45 mol/L |
14.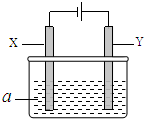 电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.
请回答以下问题:
(1)X的电极名称是阴极(填写“阳极”或“阴极”).
(2)若X、Y都是惰性电极,a是硫酸钠溶液,实验开始时,同时在两边各滴入几滴紫色石蕊试液,一段时间后,在X极附近观察到的现象是溶液变为红色,Y极上的电极反应式为4OH--4e-=H2O+O2↑.
(3)若X、Y都是惰性电极,a是AgNO3溶液,电解一段时间后,阳极上产
生气体的体积为0.448L(标准状况下),则阴极上析出金属的质量为8.64g.
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则Y电极的材料是粗铜,X电极的材料是精铜.
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是C.
 电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)X的电极名称是阴极(填写“阳极”或“阴极”).
(2)若X、Y都是惰性电极,a是硫酸钠溶液,实验开始时,同时在两边各滴入几滴紫色石蕊试液,一段时间后,在X极附近观察到的现象是溶液变为红色,Y极上的电极反应式为4OH--4e-=H2O+O2↑.
(3)若X、Y都是惰性电极,a是AgNO3溶液,电解一段时间后,阳极上产
生气体的体积为0.448L(标准状况下),则阴极上析出金属的质量为8.64g.
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则Y电极的材料是粗铜,X电极的材料是精铜.
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是C.
| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | AgNO3 |
| D | 铁 | 银 | Fe(NO3)3 |
13.将10L空气通过臭氧发生器,有部分氧气发生反应:3O2=2O3,得到9.7L混合气体,则得到臭氧的体积(同条件)是( )
| A. | 1L | B. | 0.5L | C. | 0.3L | D. | 0.6L |
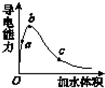 在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示,回答下列问题.
在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示,回答下列问题.