题目内容
在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρg?cm-3,溶质的质量分数为ω,溶质的物质的量浓度为c mol/L.下列叙述中正确的是( )
①ω=
×100%
②c=
③上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
④上述溶液中再加入1.5VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
①ω=
| 35a |
| 22.4Vp |
②c=
| 1000a |
| 22.4V |
③上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
④上述溶液中再加入1.5VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
分析:①溶质的质量分数为ω可由溶质的质量和溶液的质量来计算;
②根据c=
来计算;
③根据溶质的质量分数=
×100%来计算;
④根据反应后的溶质及水解来分析.
②根据c=
| n |
| V |
③根据溶质的质量分数=
| m质 |
| m液 |
④根据反应后的溶质及水解来分析.
解答:解:①VmL氨水,溶液的密度为ρg?cm-3,溶液的质量为ρVg,溶质的质量为
×17,则溶质的质量分数为ω=
×100%,故①错误;
②溶质的物质的量为
mol,溶液的体积为VmL,则c=
mol/L,故②正确;
③再加入VmL水后,所得溶液的质量分数为
,水的密度大于氨水的密度,则所得溶液的质量分数小于
0.5ω,故③错误;
④VmL氨水,再加入1.5VmL同浓度稀盐酸,充分反应后生成氯化铵,还有剩余的盐酸,溶液显酸性,
则c(Cl-)>c(NH4+)>c(H+)>c(OH-),故④正确;
故选D.
| a |
| 22.4 |
| 17a |
| 22.4Vp |
②溶质的物质的量为
| a |
| 22.4 |
| 1000a |
| 22.4V |
③再加入VmL水后,所得溶液的质量分数为
| ρVω |
| ρV+ρ水V |
0.5ω,故③错误;
④VmL氨水,再加入1.5VmL同浓度稀盐酸,充分反应后生成氯化铵,还有剩余的盐酸,溶液显酸性,
则c(Cl-)>c(NH4+)>c(H+)>c(OH-),故④正确;
故选D.
点评:本题考查物质的量浓度的有关计算,明确质量分数、物质的量浓度的关系、氨水的密度与水的密度大小是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
 (2009?长春一模)将一定质量的Mg和Al的混合物投入1mol?L-1500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )
(2009?长春一模)将一定质量的Mg和Al的混合物投入1mol?L-1500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )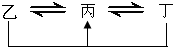 元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应.请回答下列问题:
元素A、B、C、D、E、F是位于元素周期表前四周期元素,且原子序数依次增大.其中 D、F为常见金属元素;A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为0.759g?L-1,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族,由D或F元素组成的单质或某些离子(或化合物)在溶液中均有下列转化关系(其它参与反应的物质未列出):其中,均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;均含F元素的乙、丙、丁微粒间的转化全为氧化还原反应;相邻的乙与丙或丙与丁两两间均互不发生化学反应.请回答下列问题: