题目内容
用1L1.0mol/L的KOH溶液吸收SO2气体17.92L(标准状况),所的溶液中SO32-和HSO3-的物质的量之比为 .
考点:化学方程式的有关计算
专题:计算题
分析:令SO32-和HSO3-的物质的量分别为x mol、y mol,根据钾离子守恒及S原子守恒列方程计算解答.
解答:
解:KOH的物质的量=1 L×1 mol/L=1 mol,
SO2气体的物质的量=
=0.8 mol,
令SO32-和HSO3-的物质的量分别为x mol、y mol,则:
解得x=0.2 y=0.6
故溶液中SO32-和HSO3-的物质的量之比为0.2mol:0.6mol=1:3,
故答案为:1:3.
SO2气体的物质的量=
| 17.92 L |
| 22.4L/mol |
令SO32-和HSO3-的物质的量分别为x mol、y mol,则:
|
解得x=0.2 y=0.6
故溶液中SO32-和HSO3-的物质的量之比为0.2mol:0.6mol=1:3,
故答案为:1:3.
点评:本题考查化学方程式有关计算,难度不大,注意利用元素守恒进行解答,简化计算过程.

练习册系列答案
相关题目
以1一氯丙烷为主要原料,制取1,2-丙二醇时,需要经过的各反应分别为( )
| A、加成-消去-取代 |
| B、消去-加成-取代 |
| C、取代-消去-加成 |
| D、取代-加成-消去 |
下列物质的水溶液中,加入稀H2SO4或MgCl2都有白色沉淀生成的是( )
| A、BaCl2 |
| B、Na2CO3 |
| C、KOH |
| D、Ba(OH)2 |
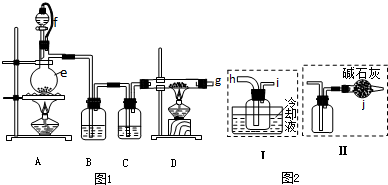
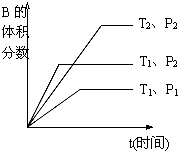 已知某可逆反应mA(g)+nB(g)?qC(g)+pD(s)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空(注:(2)、(3)、(4)题填“>”、“<”或“=”):
已知某可逆反应mA(g)+nB(g)?qC(g)+pD(s)在密闭容器中进行.如图所示反应在不同时间t,温度T和压强P与反应物B的体积分数的关系曲线.根据图象填空(注:(2)、(3)、(4)题填“>”、“<”或“=”): 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.例如二乙醚的结构简式为:CH3-CH2-O-CH2-CH3
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.例如二乙醚的结构简式为:CH3-CH2-O-CH2-CH3