题目内容
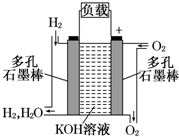
16.图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从正、负两极通入燃料电池时,便可在闭合回路中不断地产生电流.(1)图中通过负载的电子流向向右(“向左”或“向右”).
(2)写出氢氧燃料电池工作时电极反应方程式.
正极:O2+2H2O+4e-=4OH-;
负极:2H2+4OH--4e-=4H2O.
分析 (1)燃料电池中电子从负极流向正极;
(2)氢氧燃料电池中,电解质溶液为碱,则正极上氧气得电子和水生成氢氧根离子,负极上氢气失电子生成水.
解答 解:(1)燃料电池中电子从负极流向正极,通入氢气的一极为负极,通入氧气的一极为正极,则电子流动方向向右;
故答案为:向右;
(2)氢氧燃料电池中,电解质溶液为碱,则正极上氧气得电子和水生成氢氧根离子,则其电极反应式为:2H2O+O2+4e-═4OH-;负极上氢气失电子生成水,负极上电极方程式为:2H2+4OH--4e-=4H2O;
故答案为:2H2O+O2+4e-═4OH-;2H2+4OH--4e-=4H2O.
点评 本题考查学生原电池的工作原理,题目难度不大,注意把握电极的判断方法和电极方程式的书写,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
6.25℃时,浓度相同的Na2CO3和NaHCO3溶液,下列判断不正确的是( )
| A. | 粒子种类不相同 | B. | c(OH-)前者大于后者 | ||
| C. | 均存在电离平衡和水解平衡 | D. | 分别加入NaOH固体,c(CO32-)均增大 |
7.镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成.某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:

已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+,Cl2可以氧化Ni(OH)2.
②已知实验温度时的溶解度:NiC2O4>NiC2O4•H2O>NiC2O4•2H2O
③某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如下表所示:
试回答相关问题:
(1)用NiO调节溶液的pH,依次析出沉淀ⅠFe(OH)3和沉淀ⅡAl(OH)3(填化学式),调节过程中pH不能低于4.2.
(2)写出加入Na2C2O4溶液的反应的化学方程式NiCl2+Na2C2O4+2H2O═NiC2O4•2H2O↓+2NaCl.
(3)写出流程中,通入Cl2发生“氧化”反应的离子方程式2Ni(OH)2+2OH-+Cl2═2Ni(OH)3+2Cl-.
(4)如何检验Ni(OH)3已洗涤干净?取最后一次洗涤液,加入AgNO3溶液,如有白色沉淀生成,再加入稀硝酸,若沉淀不溶解,证明沉淀已洗涤干净.

已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+,Cl2可以氧化Ni(OH)2.
②已知实验温度时的溶解度:NiC2O4>NiC2O4•H2O>NiC2O4•2H2O
③某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如下表所示:
| M(OH)n | Ksp | 开始沉淀pH | 沉淀完全pH |
| Al(OH)3 | 1.9×10-23 | 3.4 | 4.2 |
| Fe(OH)3 | 3.8×10-38 | 2.5 | 2.9 |
| Ni(OH)2 | 1.6×10-14 | 7.6 | 9.8 |
(1)用NiO调节溶液的pH,依次析出沉淀ⅠFe(OH)3和沉淀ⅡAl(OH)3(填化学式),调节过程中pH不能低于4.2.
(2)写出加入Na2C2O4溶液的反应的化学方程式NiCl2+Na2C2O4+2H2O═NiC2O4•2H2O↓+2NaCl.
(3)写出流程中,通入Cl2发生“氧化”反应的离子方程式2Ni(OH)2+2OH-+Cl2═2Ni(OH)3+2Cl-.
(4)如何检验Ni(OH)3已洗涤干净?取最后一次洗涤液,加入AgNO3溶液,如有白色沉淀生成,再加入稀硝酸,若沉淀不溶解,证明沉淀已洗涤干净.
11.设nA为阿佛加德罗常数的数值,下列说法正确的是( )
| A. | 1mol/LNaCl溶液含有nA个Na+ | |
| B. | 0.1molOH-含nA个电子 | |
| C. | 1molCu和足量稀硝酸反应产生nA个NO分子 | |
| D. | 常温常压下,22.4LCO2中含有nA个CO2分子 |
1.短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Z为地壳中含量最高的金属元素.下列说法正确的是( )
| X | ||||||
| Y | Z | W |
| A. | 工业上电解YW饱和溶液冶炼金属Y | |
| B. | 气态氢化物的稳定性:W>X | |
| C. | Y、W的最高价氧化物的水化物均能溶解金属Z | |
| D. | 简单离子半径的大小顺序:r(Y+)>r(X-) |
5.在火星上工作的美国“勇气号”“机遇号”探测车的一个重要任务就是收集有关Fe2O3的信息,以证明火星上存在或曾经存在过水,以下叙述正确的是( )
| A. | 铝热剂就是单指Fe2O3 粉和铝粉 | |
| B. | 检验从火星上带回来的红色物质是否是Fe2O3的操作步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 | |
| C. | 分别还原1mol Fe2O3所需H2、Al、CO 的物质的量之比3:2:3 | |
| D. | Fe2O3和Fe3O4都是具有磁性 |
6.下列分子或离子中空间构型是V形的是( )
| A. | H3O+ | B. | H2O | C. | NO2+ | D. | NO2- |
 在常温下,Fe 与水并不发生反应,但在高温下,Fe 与水蒸气可以发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,即可以完成高温下Fe 与水蒸气的反应实验.
在常温下,Fe 与水并不发生反应,但在高温下,Fe 与水蒸气可以发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,即可以完成高温下Fe 与水蒸气的反应实验.