题目内容
13.提纯含有少量硝酸钡杂质的硝酸钾溶液,设计实验方案为:溶液$\stackrel{过量X}{→}$ $\stackrel{过滤}{→}$ $\stackrel{除去沉淀}{→}$ $\stackrel{适量硝酸}{→}$KNO3溶液则X 试剂为( )
| A. | Na2CO3 | B. | K2CO3 | C. | Na2SO4 | D. | K2SO4 |
分析 含有少量硝酸钡杂质,则X试剂除去钡离子,加过量硝酸除去试剂X,以此来解答.
解答 解:由分离实验方案可知,X试剂除去钡离子,使钡离子转化为沉淀,过滤而除去,再加过量硝酸除去试剂X,且除杂不能引入新杂质,则A、C排除,D中硫酸钾与硝酸不反应,则只有B中碳酸钾符合,
故选B.
点评 本题考查分离、提纯实验方案的设计,为高频考点,把握实验流程及混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意除杂不能引入新杂质,题目难度中等.

练习册系列答案
相关题目
4.下列说法不正确的是( )
| A. | 地球上99%溴蕴藏在大海中,故溴被称为“海洋元素” | |
| B. | 高压钠灯发出的黄光射程特别远,故常用于道路与广场的照明 | |
| C. | 碳酸氢钠可与盐酸反应,故可作治疗胃酸过多的药剂 | |
| D. | 利用光线在硅晶体内的全反射现象,可以制备光导纤维 |
1. 如图,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则关于原来H2、O2的体积比下列正确的是( )
如图,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则关于原来H2、O2的体积比下列正确的是( )
 如图,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则关于原来H2、O2的体积比下列正确的是( )
如图,密闭容器内分别充入空气和H2、O2的混合气体在可移动的活塞两边,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央,则关于原来H2、O2的体积比下列正确的是( )| A. | 4:17 | B. | 3:7 | C. | 8:13 | D. | 7:4 |
8.化学实验中安全意识是重要的科学素养,下列实验操作或事故处理操作中正确的是( )
| A. | 酒精灯不慎碰倒起火时可用水扑灭 | |
| B. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| C. | 配制硫酸溶液时,可先在量筒中加入一定量的水,再在搅拌条件下加入浓硫酸 | |
| D. | 做“氢气还原氧化铜”的实验时,先加热再通氢气 |
18.下列叙述不正确的是( )
| A. | 标准状况下,22.4LNO与11.2LO2混合,混合气体所含分子数为NA | |
| B. | 1molAl3+含有的核外电子数为10NA | |
| C. | 常温常压下,1mol氮气含有的原子总数为2NA | |
| D. | 1L1mol/LFeCl3溶液全部制成胶体,其中含胶粒的数目小于NA |
1.关于工业制硫酸的说法不正确的是( )
| A. | 燃烧硫生成SO3 | B. | SO3与水反应生成H2SO4 | ||
| C. | SO2氧化成SO3需要使用催化剂 | D. | 主要设备是沸腾炉、接触室、吸收塔 |
18.某浓度的硝酸与过量铁粉反应,生成标况下一氧化二氮气体4.48L.若改用铝反应,假设只生成一氧化氮气体,则最多可溶解铝的量( )
| A. | 13.5g | B. | 9g | C. | 27g | D. | 0.33mol |
19.已知下列热化学方程式:Zn(s)+$\frac{1}{2}$O2( )=ZnO(s);△H=-351.1kJ/mol
Hg(l)+$\frac{1}{2}$O2(g)=HgO(s);△H=-90.7kJ/mol,
由此可知反应:Zn(s)+HgO(s)=ZnO(s)+Hg(l)的△H为( )
Hg(l)+$\frac{1}{2}$O2(g)=HgO(s);△H=-90.7kJ/mol,
由此可知反应:Zn(s)+HgO(s)=ZnO(s)+Hg(l)的△H为( )
| A. | △H=-1141.8kJ/mol | B. | △H=+260.4kJ/mol | ||
| C. | △H=+441.8kJ/mol | D. | △H=-260.4kJ/mol |
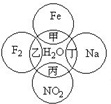 如图所示两圆圈相交的部分表示圆圈内物质间相互发生的反应,其中属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )
如图所示两圆圈相交的部分表示圆圈内物质间相互发生的反应,其中属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )