题目内容
15.有机化合物G常用作香料,合成路线如下: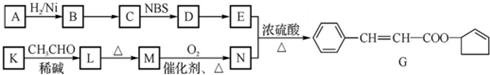
已知以下信息:
①A的分子式为C5H8O,核磁共振氢谱显示其有两种不同化学环境的氢
②CH3CH2CH=CH2$\stackrel{NBS}{→}$C H3CHBrCH=CH2
③
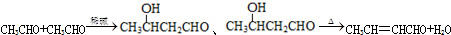
回答下列问题:
(1)K中官能团的名称为醛基.B→C的反应类型为消去反应.
(2)A的结构简式为
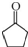
(3)M与新制氢氧化铜反应的化学方程式为
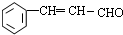 +2Cu(OH)2 $\stackrel{△}{→}$
+2Cu(OH)2 $\stackrel{△}{→}$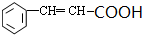 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.(4)检验M是否已完全转化为N的实验操作是取少量试样于试管中,滴加稀NaOH至溶液呈碱性,再加入新制Cu(OH)2加热至沸,若没有砖红色沉淀产生,说明M已完全转化为N,否则M未完全转化为N.
(5)满足下列条件的L的同分异构体有4种(不考虑立体异构).
①既能发生银镜反应,也能发生水解反应
②苯环上的一溴代物只有两种.
(6)结合题给信息,设计一条以1-丁醇和NBS为原料制备1,3-丁二烯的合成路线(其他试剂任选):
合成路线流程图示例:
CH3CH2Cl$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓H_{2}SO_{4}}^{CH_{3}COOH}$CH3COOCH2CH3.
分析 由G的结构简式可知E、N分别为 、
、 中的一种,K发生信息③中的转化得到M,M发生催化氧化生成N为羧酸,故N为
中的一种,K发生信息③中的转化得到M,M发生催化氧化生成N为羧酸,故N为 ,E为
,E为 ,逆推可知M为
,逆推可知M为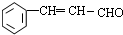 ,L为
,L为 ,K为
,K为 .A的分子式为C5H8O,核磁共振氢谱显示其有两种不同化学环境的氢,能与氢气发生加成反应,系列转化得到E,可知A为
.A的分子式为C5H8O,核磁共振氢谱显示其有两种不同化学环境的氢,能与氢气发生加成反应,系列转化得到E,可知A为 ,则B为
,则B为 ,结合信息②可知,B发生消去反应生成C为
,结合信息②可知,B发生消去反应生成C为 ,C与NBS发生取代反应生成D为
,C与NBS发生取代反应生成D为 ,D在氢氧化钠水溶液、加热条件下发生水解反应生成E;
,D在氢氧化钠水溶液、加热条件下发生水解反应生成E;
(6)1-丁醇发生消去反应生成1-丁烯,1-丁烯发生信息②的反应生成CH3CHBrCH=CH2,CH3CHBrCH=CH2发生消去反应生成1,3-丁二烯.
解答 解:由G的结构简式可知E、N分别为 、
、 中的一种,K发生信息③中的转化得到M,M发生催化氧化生成N为羧酸,故N为
中的一种,K发生信息③中的转化得到M,M发生催化氧化生成N为羧酸,故N为 ,E为
,E为 ,逆推可知M为
,逆推可知M为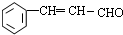 ,L为
,L为 ,K为
,K为 .A的分子式为C5H8O,核磁共振氢谱显示其有两种不同化学环境的氢,能与氢气发生加成反应,系列转化得到E,可知A为
.A的分子式为C5H8O,核磁共振氢谱显示其有两种不同化学环境的氢,能与氢气发生加成反应,系列转化得到E,可知A为 ,则B为
,则B为 ,结合信息②可知,B发生消去反应生成C为
,结合信息②可知,B发生消去反应生成C为 ,C与NBS发生取代反应生成D为
,C与NBS发生取代反应生成D为 ,D在氢氧化钠水溶液、加热条件下发生水解反应生成E;
,D在氢氧化钠水溶液、加热条件下发生水解反应生成E;
(1)K为 ,K中官能团的名称为醛基,B→C的反应类型为消去反应,故答案为:醛基;消去反应;
,K中官能团的名称为醛基,B→C的反应类型为消去反应,故答案为:醛基;消去反应;
(2)A的结构简式为 ,故答案为:
,故答案为: ;
;
(3)M为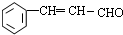 ,
,
M与新制氢氧化铜反应的化学方程式为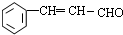 +2Cu(OH)2 $\stackrel{△}{→}$
+2Cu(OH)2 $\stackrel{△}{→}$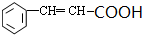 +Cu2O↓+3H2O,
+Cu2O↓+3H2O,
故答案为: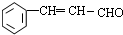 +2Cu(OH)2 $\stackrel{△}{→}$
+2Cu(OH)2 $\stackrel{△}{→}$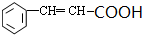 +Cu2O↓+3H2O;
+Cu2O↓+3H2O;
(4)M转化为N是醛基转化为羧基,可以检验反应后物质是否含有醛基判断M是否已完全转化为N,实验操作是:取少量试样于试管中,滴加稀NaOH至溶液呈碱性,再加入新制Cu(OH)2加热至沸,若没有砖红色沉淀产生,说明M已完全转化为N,否则M未完全转化为N,
故答案为:取少量试样于试管中,滴加稀NaOH至溶液呈碱性,再加入新制Cu(OH)2加热至沸,若没有砖红色沉淀产生,说明M已完全转化为N,否则M未完全转化为N;
(5)L为 ,L的同分异构体满足下列条件,
,L的同分异构体满足下列条件,
①既能发生银镜反应,也能发生水解反应,说明含有酯基和醛基,应该为甲酸酯;
②苯环上的一溴代物只有两种,说明苯环上只有两种氢原子,
取代基为HCOOCH2-、-CH3,且处于对位;
取代基为HCOO-、-CH2CH3,且处于对位;
取代基为HCOO-、2个-CH3,两个甲基相间且中间为HCOO-,有一种结构;
取代基为HCOO-、2个-CH3,两个甲基相间且HCOO-和两个甲基处于相间位置,有一种结构;
符合条件的有四种,
故答案为:4;
(6)1-丁醇发生消去反应生成1-丁烯,1-丁烯发生信息②的反应生成CH3CHBrCH=CH2,CH3CHBrCH=CH2发生消去反应生成1,3-丁二烯,合成路线为CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2,
故答案为:CH3CH2CH2CH2OH$→_{△}^{浓硫酸}$CH3CH2CH=CH2$\stackrel{NBS}{→}$CH3CHBrCH=CH2$→_{△}^{NaOH醇溶液}$CH2=CHCH=CH2.
点评 本题考查有机物的推断和合成,为高频考点,侧重考查学生分析判断及知识综合应用、知识迁移能力,把握有机物官能团的性质、位置之间的转化是解本题关键,注意醛发生加成反应断键和成键位置,为易错点.

Ⅰ.探究过氧化氢的性质
(1)该化学小组设计了两个实验,分别证明了H2O2的两个性质.请将他们的实验现象和验证性质填入下表:
| 实验所用试剂或操作 | 实 验 现 象 | 验证的性质 |
| 碘化钾淀粉溶液 | ||
| 取适量过氧化氢溶液于试管中,加热,用带火星的木条检验. |
2Fe2++H2O2+2H+=2Fe3++2H2O,2Fe3++H2O2=2Fe2++O2↑+2H+下列说法正确的是ACD
A.H2O2的氧化性比Fe3+强,其还原性比Fe2+强
B.在H2O2分解过程中,溶液的pH逐渐下降
C.在H2O2分解过程中,Fe2+和Fe3+的总量发生变化
D.H2O2生产过程要严格避免混入Fe2+
Ⅱ.测定过氧化氢的含量
(1)量取10.00mL密度为ρ g/mL的过氧化氢溶液,溶解后将溶液转移至250mL容量瓶(填仪器名称)中,加水稀释至刻度,摇匀.移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样.
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里.□MnO4-+□H2O2+□H+=□Mn2++□H2O+□□
该反应体现了H2O2的还原性.
(3)滴定时,将高锰酸钾标准溶液注入酸式 (填“酸式”或“碱式”)滴定管中.滴定到达终点的现象是滴入一滴高锰酸钾溶液,溶液呈浅红色,且30秒内不褪色.
(4)反复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为$\frac{0.085cV}{ρ}$.
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果偏高(填“偏高”或“偏低”或“不变”).
| A. | 乙醇是食醋的主要成分 | |
| B. | C2H5OH中C、H、O元素的质量比是2:6:1 | |
| C. | 乙醇不能溶于水 | |
| D. | C2H5OH中C元素的质量分数是$\frac{12×2}{12×2+1×6+16×1}$ |
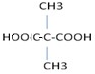 .
. 00 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图中曲线所示。下列分析正确的是
00 mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图中曲线所示。下列分析正确的是
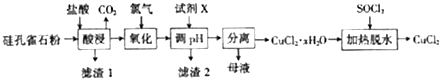
 .
. 或
或 .
.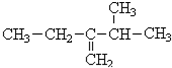 2-乙基-3-甲基-1-丁烯;
2-乙基-3-甲基-1-丁烯;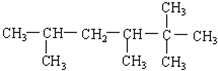 2,2,3,5-四甲基己烷.
2,2,3,5-四甲基己烷.