题目内容
6.X、Y、Z、W四种元素都是短周期元素,且原子序数W>Z>Y>X.已知:X与Y的原子的最外层电子数之和与Z原子最外层电子数相等;X的阳离子半径是自然界中离子半径最小的;W和 Y原子的最外层电子数之和是Z原子最外层电子数的2倍;W原子的最外层电子数为其电子层数 的3倍.试回答:?(1)写出元素符号:XH、YC、ZN、WO.?
(2)上述元素单质中熔点最高的是C.(用化学式表示)?
(3)写出Y与W构成的最高价化合物的电子式
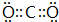
(4)由上述四种元素组成的离子化合物在300℃完全分解为气态混合物,且混合气体的平均相对分子质量为24.该离子化合物的化学式是(NH4)2CO3.
分析 X、Y、Z、W四种元素都是短周期元素,且原子序数W>Z>Y>X.X的阳离子半径是自然界中离子半径最小的,则X为H元素;W原子的最外层电子数为其电子层数 的3倍,原子只能有2个电子层,最外层电子数为6,故E为O元素;结合原子序数可知Y、Z处于第二周期,X(氢)与Y的原子的最外层电子数之和与Z原子最外层电子数相等,则Y、Z相邻,W和 Y原子的最外层电子数之和是Z原子最外层电子数的2倍,设Y最外层电子数为x,则Z的最外层电子数为x+1,故8+x=2(x+1),解得x=6,故Y为C元素,Z为N元素.
解答 解:X、Y、Z、W四种元素都是短周期元素,且原子序数W>Z>Y>X.X的阳离子半径是自然界中离子半径最小的,则X为H元素;W原子的最外层电子数为其电子层数 的3倍,原子只能有2个电子层,最外层电子数为6,故E为O元素;结合原子序数可知Y、Z处于第二周期,X(氢)与Y的原子的最外层电子数之和与Z原子最外层电子数相等,则Y、Z相邻,W和 Y原子的最外层电子数之和是Z原子最外层电子数的2倍,设Y最外层电子数为x,则Z的最外层电子数为x+1,故8+x=2(x+1),解得x=6,故Y为C元素,Z为N元素.
(1)由上述分析可知,X为H、Y为C、Z为N、W为O,
故答案为:H;C;N;O;?
(2)上述元素单质中碳元素单质为固体,其它单质均为气体,故碳元素单质的熔点最高,
故答案为:C;?
(3)Y与W构成的最高价化合物为CO2,电子式为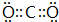 ,
,
故答案为: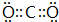 ;
;
(4)由上述四种元素组成的离子化合物在300℃完全分解为气态混合物,常见化合物中碳酸铵、碳酸氢铵等符合,且混合气体的平均相对分子质量为24,1mol碳酸氢铵分解得到1mol氨气、1mol水蒸气、1mol二氧化碳,平均相对分子质量为$\frac{79}{3}$=26.3,不符合题意,而1mol碳酸铵分解得到2mol氨气、1mol水蒸气、1mol二氧化碳,平均相对分子质量为$\frac{96}{4}$=24,符合题意,故该离子化合物的化学式是(NH4)2CO3,
故答案为:(NH4)2CO3.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,(4)为本题的难点,由四种元素形成的离子化合物很多,通过猜测验证进行解答.

 全能测控期末小状元系列答案
全能测控期末小状元系列答案 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案| A. | 8 | B. | 9 | C. | 11 | D. | 14 |
| X | Y | Z | |
| R | |||
| W | |||
| J |
(1)R原子的电子排布图为
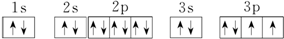 .
.(2)在化合物YZ2中Y的化合价为+2;Y2-与Na+的半径大小为O2->Na+.
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是F>O>N;X与Y的第一电离能:X>Y(填“<”、“>”或“=”),其理由是N原子的p轨道为半充满,能量低较稳定,难失电子.
(2)下列有关蒸馏乙醇和提纯苯甲酸实验的判断不正确的有b;
a.蒸馏乙醇的主要仪器有蒸馏烧瓶、温度计、冷凝管、铁架台、酒精灯、接液管和锥形瓶
b.如果温度计水银球位置低于支管口下沿,则收集的乙醇含有低沸点杂质
c.提纯苯甲酸时,用热水溶解,冷却后过滤除去固体杂质
d.测定苯甲酸晶体的熔点可能判断苯甲酸晶体是否为纯净物
(3)两种有机物A和B可以互溶,有关性质如下:
| 相对密度(20℃) | 熔点 | 沸点 | 溶解性 | |
| A | 0.7893 | -117.3°C | 78.5°C | 与水以任意比混溶 |
| B | 0.7137 | -116.6°C | 34.5°C | 不溶于水 |
a.重结晶 b.蒸馏 c.萃取 d.加水充分振荡,分液.
| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
| A. | 均含共价键 | B. | 性质相同 | C. | 互为同位素 | D. | 互为同分异构体 |
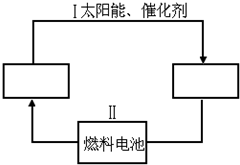 能源可化分为一级能源和二级能源.自然界以现成方式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,而如何快速制取出大量的氢气则成为发展氢能源的主要问题.
能源可化分为一级能源和二级能源.自然界以现成方式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,而如何快速制取出大量的氢气则成为发展氢能源的主要问题. .
.
 ;
;