��Ŀ����
4��Ϊ��̽�����Ʊ�����ˮ����ɺ����ʶ����������п�ѧʵ�飬�����Ҫ��ش����⣺��1����д�����Ʊ�����ˮ�к�����Ԫ�ص����ʵĻ�ѧʽ��HCl��HClO��Cl2��
��2�������ٽ��и����ʵ�飬��˵���ܿ����ж���ˮ�к���Cl2����Ҫ������ˮ��dz����ɫ��
��3�����Ƶı�����ˮ�е�����������Һ������Ϊ��ɫ������������ɫʯ����ֽ�ϵ�����Ϊ�ȱ�����ɫ�������īˮ�е�����Ϊ��ɫ��
���� ��1�����ݷ�ӦCl2+H2O=HCl+HClO�жϣ�
��2��������ˮ����ɫ�����������������ɫ��
��3��Cl2+H2O?HCl+HClO������������ˮ�д���Cl2��HClO��H2O��H+��Cl-��ClO-��OH-���������ʵ��������������
������ˮ��Һ�д��������ӣ����Ե�����������Һ������ɫ�Ȼ���������
������ˮ��Һ�д��ڴ����ᣬ��Ư���ԣ�������ɫʯ����ֽ�ϣ��ȱ�죬����ɫ��
������ˮ��Һ�д��ڴ����ᣬ��Ư���ԣ������īˮ��ɫ��ȥ��
��� �⣺��1��������ˮ��Ӧ������Cl2+H2O=HCl+HClO�����Ʊ�����ˮ�к�����Ԫ�ص�����ΪHCl��HClO��Cl2���ʴ�Ϊ��HCl��HClO��Cl2��
��2��������ˮ��dz����ɫ����ˮ�к�����Ԫ�ص�����ΪHCl��HClO��Cl2������HCl��HClO��ɫ��˵�������������ӣ��ʴ�Ϊ����ˮ��dz����ɫ��
��3��Cl2+H2O?HCl+HClO������������ˮ�д���Cl2��HClO��H2O��H+��Cl-��ClO-��OH-����ˮ�к���HClO��Cl2�����������ԣ�����HClO����Ư���ԣ�����H+���������ԣ�
����AgNO3��Һ��������ˮ��Һ�е������Ӻ�������������������ӷ�Ӧ�����Ȼ�����ɫ������Ag++Cl-�TAgCl����
������ɫʯ����ֽ�ϣ�������ˮ��Һ�е�����ʹʯ���죬������ˮ��Һ�д��ڴ��������ǿ�����ԣ�����Ư���ԣ���Ư���Ծ��в������ԣ����Ժ���ɫ��
������ˮ��Һ�д��ڴ����ᣬ��Ư���ԣ������īˮ����ɫ��ȥ��
�ʴ�Ϊ����ɫ�������ȱ�����ɫ����ɫ��
���� ���⿼����������ˮ�����ʣ���ȷ��ˮ�д��ڵijɷּ����ɷֵ����ʡ��ر�����ȷ�����������ᵫ����ǿ�����������Ư�����ǽ����Ĺؼ�����Ŀ�ѶȲ���

 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д�| A�� | �������� | B�� | �������� | C�� | �������� | D�� | ������ |
| A�� | 2-��-5-�һ����� | B�� | 3��3-����-2-��ϩ | ||
| C�� | 3-��-2-��ϩ | D�� | 2��2-�������� |
| A�� | ���ʵ��۵㣺Y��Z��X | B�� | ���⻯����ȶ��ԣ�X��R��Z | ||
| C�� | �����Ӱ뾶��Y��R��X | D�� | X������3��Ԫ�ض�������ӻ����� |
���Բ���ȷ���ǣ�������
| A�� | ��ɢϵ�ķ��� | B�� | 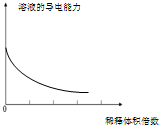 ϡ��Ũ����������Һ�Ĺ��� | ||
| C�� | 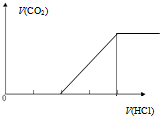 ��̼������Һ����εμ����� | D�� | 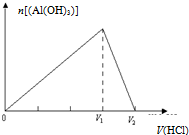 ��ƫ��������Һ����εμ����� |
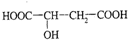 ��
��


 ����ӦA���Ȼ�ѧ����ʽ��4HCl��g��+O2��g��?2Cl2��g��+2H2O��g����H=-115.6 KJ/mol��
����ӦA���Ȼ�ѧ����ʽ��4HCl��g��+O2��g��?2Cl2��g��+2H2O��g����H=-115.6 KJ/mol��