题目内容
17.写出下列物质的空间立体构型(1)H2SV型;
(2)CO2直线形;
(3)NH3三角锥型.
分析 根据价层电子对互斥理论确定其空间构型,价层电子对个数=σ键个数+孤电子对个数,据此分析解答.
解答 解:(1)H2S分子中价层电子对个数=σ键个数+孤电子对个数=2+2=4,而中心原子外围只有两个原子所以含有2个孤电子对,即H2S为V型结构,
故答案为:V型;
(2)CO2分子中每个O原子和C原子形成两个共用电子对,所以C原子价层电子对个数是2,且不含孤电子对,所以为直线形结构,
故答案为:直线形;
(3)NH3分子中心N原子孤电子对数=$\frac{5-1×3}{2}$=1,价层电子对数=3+1=4,故N原子采取sp3杂化,含1对孤电子,所以分子的立体构型为三角锥型,
故答案为:三角锥型.
点评 本题考查了粒子空间构型的判断,根据价层电子对互斥理论来分析解答即可,注意孤电子对个数的计算方法,为易错点,题目难度不大.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
1.有机物 的正确命名为( )
的正确命名为( )
 的正确命名为( )
的正确命名为( )| A. | 2,3,3-三甲基戊烷 | B. | 3,3,4-三甲基已烷 | ||
| C. | 3,3-二甲基-4-乙基戊烷 | D. | 2-乙基-3,3-二甲基-4-乙基戊烷 |
5.东晋医药学家葛洪的《肘后备急方•治寒热诸疟方》记载有“青蒿一握,以水二升渍,绞取汁,尽服之”用沸点只有35℃的乙醚作为溶剂来提取青蒿素的方法化学上叫萃取的说法,说明不能加热青蒿,因高温可能使活性成分受损.中国药学家屠呦呦用沸点只有35℃的乙醚作为溶剂来提取青蒿素,创制出新型抗疟药青蒿素和双氢青蒿素,为此获得2015年诺贝尔生理学或医学奖.已知青蒿素的结构如图所示,下列有关青蒿素的说法,不正确的是( )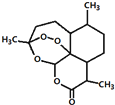

| A. | 用沸点只有35℃的乙醚作为溶剂来提取青蒿素的方法化学上叫萃取 | |
| B. | 能够发生水解反应 | |
| C. | 分子式为C15H23O5 | |
| D. | 青蒿素能够治疗疟疾可能与结构中存在过氧键或酯基等基团有关 |
12.某溶液中可能含有下列四种离子,加入KSCN溶液后变成红色,则原溶液中一定含有( )
| A. | K+ | B. | Al3+ | C. | Cl- | D. | Fe3+ |
2.短周期主族元素X、Y、Z、W的原子序数依次增大,且原子的最外层电子数之和为19.X的气态氢化物可与其最高价含氧酸反应生成离子化合物,Z+与Y2-具有相同的电子层结构.下列说法不正确的是( )
| A. | 工业上电解熔融的ZW制备Z单质 | |
| B. | 元素Y与Z形成的化合物中只能有一种化学键 | |
| C. | 离子半径大小顺序为W>X>Y>Z | |
| D. | 在一定条件下X的氢化物能与Y单质发生置换反应 |
9.下列性质比较结果错误的是( )
| A. | 碳碳键键长:乙烯>苯 | B. | 沸点:正戊烷>异戊烷 | ||
| C. | 相对密度: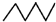 > >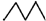 | D. | 水溶性:CH3CH2OH>CH3CH2Br |
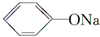 +CH3I→
+CH3I→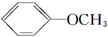 +NaI
+NaI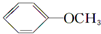 +HI→
+HI→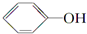 +CH3l
+CH3l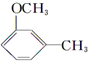 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$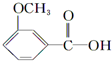
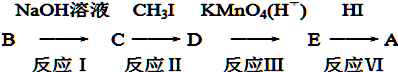
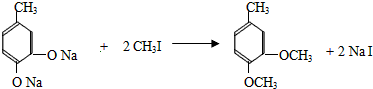 .
. .
.