题目内容
16.实验室在配制硫酸亚铁溶液时,先把硫酸亚铁晶体溶解在稀硫酸中,再加水稀释到所需的浓度,这样操作的目的是( )| A. | 提高硫酸亚铁的溶解度 | B. | 防止硫酸亚铁分解 | ||
| C. | 抑制硫酸亚铁水解 | D. | 稀硫酸防止硫酸亚铁被氧化 |
分析 实验室在配制硫酸亚铁溶液时,亚铁离子水解生成氢氧化亚铁变浑浊,先把硫酸亚铁晶体溶解在稀硫酸中,硫酸抑制亚铁离子的水解,再加水稀释至所需浓度,得到较纯净的硫酸亚铁溶液,据此解答.
解答 解:因为亚铁离子会水解,生成氢氧化亚铁,Fe2++2H2O?Fe(OH)2+2H+;加入硫酸的目的是在溶液里面形成一种酸性条件,依据平衡移动原理可知,增大氢离子浓度,平衡逆向移动,抑制氢氧化亚铁的生成,使得所配的溶液不会有沉淀,得到较纯净的硫酸亚铁溶液;
故选:C.
点评 本题考查了溶液配制,熟悉盐类水解的应用,水解平衡的影响因素分析是解题关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列关于判断过程的方向的说法正确的是( )
| A. | 常温时不能发生的过程都是非自发过程 | |
| B. | 体系的无序性越高,即混乱度越高,熵值就越大 | |
| C. | 所有自发进行的化学反应都是放热反应 | |
| D. | 同一物质的固、液、气三种状态的熵值相同 |
1.有关热化学方程式书写与对应表述均正确的是( )
| A. | 已知2C(s)+O2(g)=2CO(g)△H=-221 kJ•mol-1,则可知C的标准燃烧热为110.5 kJ•mol-1 | |
| B. | 在101KPa下氢气的标准燃烧热△H=-285.5 kJ•mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| C. | 稀硫酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ•mol-1 | |
| D. | 密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量.则Fe(s)+S(g)=FeS(s)△H=-95.6 kJ•mol-1 |
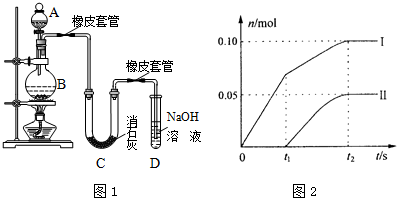

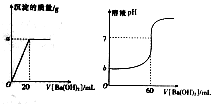 室温下,某同学为测量硫酸和盐酸混合溶液中溶质的浓度进行如下实验:取混合酸20mL放入锥形瓶中,逐滴滴人0.05mol•L-1的Ba(OH)2溶液,实验记录如下:(1g3=0.5)
室温下,某同学为测量硫酸和盐酸混合溶液中溶质的浓度进行如下实验:取混合酸20mL放入锥形瓶中,逐滴滴人0.05mol•L-1的Ba(OH)2溶液,实验记录如下:(1g3=0.5)
 +CaCl2+H2O,该反应的原子利用率25.4%.
+CaCl2+H2O,该反应的原子利用率25.4%.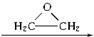 HO-CH2-CH2-O-CH2-CH2-OH
HO-CH2-CH2-O-CH2-CH2-OH