题目内容
6.下列说法不正确的是( )| A. | 金刚石和石墨互为同素异形体 | |
| B. | CH3-CH2OH和 CH3-O-CH3互为同分异构体 | |
| C. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He互为同位素 | |
| D. | 分子式为C4H10的物质为纯净物 |
分析 A.由同种元素组成的不同单质则互为同素异形体;
B.分子式相同结构不同的有机化合物互称同分异构体;
C.同一元素的不同原子互称同位素;
D.C4H10可能为正丁烷或异丁烷.
解答 解:A.金刚石和石墨都是由碳元素组成,且都是单质,则互为同素异形体,故A正确;
B.CH3-CH2OH和 CH3-O-CH3分子式相同结构不同,互为同分异构体,故B正确;
C.${\;}_{2}^{3}$He和${\;}_{2}^{4}$He质子数相同,中子数不同,互为同位素,故C正确;
D.C4H10可能为正丁烷或异丁烷,为混合物,故D错误.
故选D.
点评 本题考查化学“五同”比较,难度较小,清楚概念的内涵与外延.

练习册系列答案
相关题目
20.下列6个转化,其中不能通过一步反应实现的是( )
①SiO2→Na2SiO3 ②Fe(OH)2→Fe(OH)3 ③SiO2→H2SiO3
④Al2O3→Al(OH)3 ⑤Ca(OH)2→NaOH ⑥NaAlO2→AlCl3.
①SiO2→Na2SiO3 ②Fe(OH)2→Fe(OH)3 ③SiO2→H2SiO3
④Al2O3→Al(OH)3 ⑤Ca(OH)2→NaOH ⑥NaAlO2→AlCl3.
| A. | ①② | B. | ③④ | C. | ③④⑤ | D. | ⑤⑥ |
17.某实验小组依据反应AsO43-+2H++2I-?AsO33-+I2+H2O设计如图1原电池,探究pH对AsO43-氧化性的影响.测得电压与pH的关系如图2.下列有关叙述错误的是( )
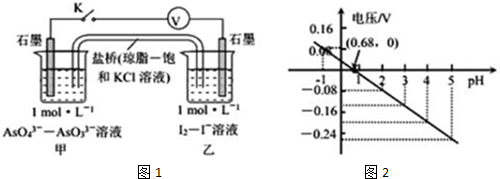

| A. | pH>0.68时,甲烧杯中石墨为负极 | |
| B. | pH=0.68时,反应处于平衡状态 | |
| C. | pH<0.68时,氧化性I2<AsO43- | |
| D. | pH=5时,负极电极反应式为2I--2e-=I2 |
14.下列化学用语正确的是( )
| A. | 乙烯的实验式:C2H4 | B. | 四氯化碳分子的电子式为: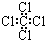 | ||
| C. | 聚丙烯的结构简式为: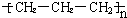 | D. | 异丁烷分子的键线式为: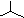 |
11.CO2气体在一定条件下可与金属镁反应,干冰在一定条件下也可以形成CO2气体,这两个变化过程中需要克服的作用分别是( )
| A. | 分子间作用力,离子键 | B. | 化学键,分子间作用力 | ||
| C. | 化学键,化学键 | D. | 分子间作用力,分子间作用力 |
18.对于乙醇分子下列说法正确的是( )
| A. | 红外光谱可确定分子内有O-H键、C-H键和C-O键 | |
| B. | 核磁共振氢谱有二个吸收峰 | |
| C. | 乙醇属于电解质 | |
| D. | 根据乙醇燃烧产物的种类可确定乙醇中含有碳、氢、氧元素 |
16.固体NH5属离子化合物,它与水反应的方程式为:NH5+H2O═NH3•H2O+H2↑,它也能跟乙醇、乙酸、盐酸等发生类似的反应,并都产生氢气.下列有关NH5叙述正确的是( )
| A. | 1mol NH5中含有3NA个N-H键 | |
| B. | NH5中N元素的化合价为-5价 | |
| C. | 1mol NH5与水反应时,转移电子为NA | |
| D. | 与乙酸反应时,NH5被还原 |