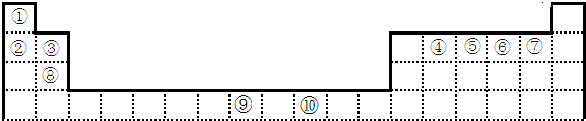
题目内容
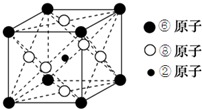
 (1)实验测得:在室温下1L水中只有10-7mol的水电离,列式计算水的电离平衡常数KH2O;
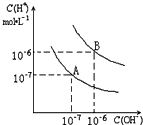
(1)实验测得:在室温下1L水中只有10-7mol的水电离,列式计算水的电离平衡常数KH2O;(2)已知水在25℃和100℃时,其电离平衡曲线如图所示,则25℃时水的电离平衡曲线应为
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:(1)根据水的电离方程式结合电离平衡常数表达式进行计算;
(2)横轴是氢氧根离子浓度,纵轴是氢离子浓度,水的离子积常数Kw=c(H+)×c(OH-)计算出A曲线的Kw值结合水的电离时吸热比较判断25℃时水的电离平衡曲线;
(2)横轴是氢氧根离子浓度,纵轴是氢离子浓度,水的离子积常数Kw=c(H+)×c(OH-)计算出A曲线的Kw值结合水的电离时吸热比较判断25℃时水的电离平衡曲线;
解答:
解:(1)由1L水中只有10-7mol的水电离,则电离生成的氢离子浓度为1.0×10-7mol/L,氢氧根离子浓度为1.0×10-7mol/L
,所以水的电离平衡常数KH2O=c(H+)×c(OH-)=10-14,答:在室温下水的电离平衡常数KH2O为1.0×10-14;
(2)曲线A条件下Kw=c(H+)×c(OH-)=10-7×10-7=10-14,曲线B条件下c(H+)=c(OH-)=10-6 mol/L,Kw=c(H+)?c(OH-)=10-12 ;水的电离时吸热过程,加热促进电离,所以A曲线代表25℃时水的电离平衡曲线,故答案为:A;温度升高促进水的电离 Kw增大;
,所以水的电离平衡常数KH2O=c(H+)×c(OH-)=10-14,答:在室温下水的电离平衡常数KH2O为1.0×10-14;
(2)曲线A条件下Kw=c(H+)×c(OH-)=10-7×10-7=10-14,曲线B条件下c(H+)=c(OH-)=10-6 mol/L,Kw=c(H+)?c(OH-)=10-12 ;水的电离时吸热过程,加热促进电离,所以A曲线代表25℃时水的电离平衡曲线,故答案为:A;温度升高促进水的电离 Kw增大;
点评:本题考查了水的电离平衡、水的离子积常数的影响因素以及计算等知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
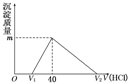 某固体物质和某溶液在一定条件下反应,产生气体的相对分子质量(或平均相对分子质量)为45,则发生反应的物质一定不可能是( )
某固体物质和某溶液在一定条件下反应,产生气体的相对分子质量(或平均相对分子质量)为45,则发生反应的物质一定不可能是( )| A、Zn和浓H2SO4 |
| B、Na2O2和NH4Cl浓溶液 |
| C、Cu和浓HNO3 |
| D、C和浓HNO3 |
60mL 0.5mol/L的氢氧化钠溶液和40mL 0.4mol/L的硫酸相混合后,溶液的pH约为( )
| A、0.5 | B、1.7 |
| C、2 | D、13.2 |
下列叙述正确的是( )
| A、CO2的摩尔质量为44g |
| B、5.4gH2O中有1.806×1023个原子 |
| C、CH4的相对分子质量为16g |
| D、2mol Cl2和2mol CO2所含分子数相等 |
下列有关化学用语表示正确的是( )
| A、二氧化硅的分子式:SiO2 | ||
B、2-乙基丁烷: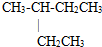 | ||
C、次氯酸的电子式: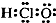 | ||
D、质子数为53,中子数为78的碘原子:
|
标准状况下有①6.72L甲烷 ②3.01×1023个氯化氢分子 ③13.6g硫化氢④0.2mol NH3.下列对这四种气体的关系从小到大表示不正确的是( )
| A、体积:④<①<②<③ |
| B、密度:①<④<③<② |
| C、质量:④<①<③<② |
| D、氢原子数:②<④<③<① |