题目内容
17.在生产、保存、运输和使用浓硝酸时,下列说法不正确的是( )| A. | 工业制取硝酸时生成的NO可循环使用 | |
| B. | 常温下,可选用铁制或铝制容器盛装 | |
| C. | 盛装容器的标签上应标注氧化剂和腐蚀品 | |
| D. | 使用时向96%的硝酸加水稀释可制得稀硝酸 |
分析 A.NO可生成二氧化氮,二氧化氮和水反应可生成硝酸;
B.浓硝酸与铁、铝在常温下发生钝化反应;
C.浓硝酸具有强氧化性和腐蚀性;
D.浓硝酸的浓度一般为69%.
解答 解:A.NO可生成二氧化氮,二氧化氮和水反应可生成硝酸,所以工业制取硝酸时生成的NO可循环使用,故A正确;
B.浓硝酸与铁、铝在常温下发生钝化反应,在表面生成一层致密的氧化膜,故B正确;
C.浓硝酸具有强氧化性和腐蚀性,则盛装容器的标签上应标注氧化剂和腐蚀品,故C正确;
D.浓硝酸易挥发、分解,浓度一般为69%,故D错误.
故选D.
点评 本题考查硝酸的性质,为高频考点,侧重于学生的双基以及分析能力的考查,有利于培养学生良好的科学素养,提高学习的积极性,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
8.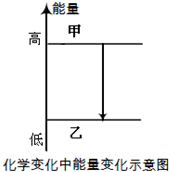 已知将甲醇蒸气转化为氢气的反应原理是:CH3OH(g)+$\frac{1}{2}$O2(g)→CO2(g)+2H2(g)+192.9kJ,下列说法正确的是( )
已知将甲醇蒸气转化为氢气的反应原理是:CH3OH(g)+$\frac{1}{2}$O2(g)→CO2(g)+2H2(g)+192.9kJ,下列说法正确的是( )
 已知将甲醇蒸气转化为氢气的反应原理是:CH3OH(g)+$\frac{1}{2}$O2(g)→CO2(g)+2H2(g)+192.9kJ,下列说法正确的是( )
已知将甲醇蒸气转化为氢气的反应原理是:CH3OH(g)+$\frac{1}{2}$O2(g)→CO2(g)+2H2(g)+192.9kJ,下列说法正确的是( )| A. | 1 g CH3OH(g)完全燃烧放出192.9 kJ的热量 | |
| B. | 1 mol CH3OH(l)完全燃烧放出的热量大于192.9 kJ | |
| C. | 图中甲为CH3OH(g)+$\frac{1}{2}$O2(g),乙为CO2(g)+2H2(g) | |
| D. | CH3OH转变成H2的过程需要吸收能量 |
5.设NA表示阿伏加德罗常数,下列说法中错误的是( )
| A. | 常温常压下,22.4L氮气所含分子数小于NA个 | |
| B. | 1molCl2通入足量水中电子转移数为NA个 | |
| C. | 1molSiO2中含有4 molSi-O键 | |
| D. | 12g金刚石含有NA个碳原子 |
12.据报道,用10B合成的10B20有非常好的抗癌效果.下列叙述正确的是( )
| A. | 10B和10B20互为同素异形体 | B. | B元素的质量数是10 | ||
| C. | 10B的中子数和核外电子数相等 | D. | 10B20晶体熔点高、硬度大 |
2.地壳中含量最多的元素在周期表中的位置是( )
| A. | 第二周期VIA族 | B. | 第二周期VA族 | C. | 第三周期VIA族 | D. | 第三周期VA族 |
9.设NA为阿伏伽德罗常数,下列说法正确的是( )
| A. | 1molFeI2与足量的氯气反应时转移的电子数为2NA | |
| B. | 常温下,34gNH3含有6NA个N-H共价键 | |
| C. | 1molNa2O2中含有的离子总数为4NA | |
| D. | 标准状况下,16gCH4与22.4LH2O含有的电子数均为10NA |
6.下列各组离子在指定介质中一定能大量共存的是( )
| A. | 在AlCl3溶液中:NH${\;}_{4}^{+}$、Fe2+、AlO${\;}_{2}^{-}$、SO${\;}_{4}^{2-}$ | |
| B. | 在AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$=8的溶液中:Al3+、Fe3+、Cl-、Br- | |
| C. | 常温下,含SO2的饱和溶液中:H+、Ca2+、MnO${\;}_{4}^{-}$、I- | |
| D. | 常温下,由水电离出的c(H+)•c(OH-)=1×10-22的溶液中:Na+、Ba2+、HCO${\;}_{3}^{-}$、NO${\;}_{3}^{-}$ |
20. 2011国际化学年,为纪念瑞士化学家Reichstein 1933年首先合成维生素C,瑞士发行了一枚印有Vc分子(C6H8O6)的3D效果邮票(如右图,图中小短棍可表示单键、双键或叁键).下列关于Vc说法正确的是( )
2011国际化学年,为纪念瑞士化学家Reichstein 1933年首先合成维生素C,瑞士发行了一枚印有Vc分子(C6H8O6)的3D效果邮票(如右图,图中小短棍可表示单键、双键或叁键).下列关于Vc说法正确的是( )
 2011国际化学年,为纪念瑞士化学家Reichstein 1933年首先合成维生素C,瑞士发行了一枚印有Vc分子(C6H8O6)的3D效果邮票(如右图,图中小短棍可表示单键、双键或叁键).下列关于Vc说法正确的是( )
2011国际化学年,为纪念瑞士化学家Reichstein 1933年首先合成维生素C,瑞士发行了一枚印有Vc分子(C6H8O6)的3D效果邮票(如右图,图中小短棍可表示单键、双键或叁键).下列关于Vc说法正确的是( )| A. | 维生素C结构中包含了一个五元碳环 | |
| B. | 从结构来看,维生素C不溶于水 | |
| C. | 维生素C具有羟基和酯基两种官能团 | |
| D. | 维生素C能与氢气、溴水、氢氧化钠溶液等发生反应 |