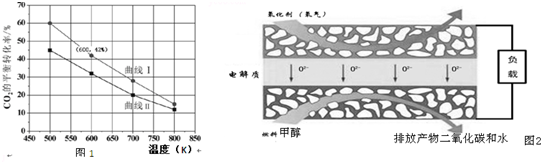
题目内容
1.铝电池性能优越,Al-空气燃料电池通常以NaCl溶液或KOH溶液为电解质溶液,通入空气的电极为正极,以多孔石墨为正极材料.若以NaCl溶液为电解质溶液,正极的反应式为O2+2H2O+4e-=4OH-;若以KOH溶液为电解质溶液,电池总反应为4Al+3O2+4KOH=4KAlO2+2H2O.分析 原电池中,负极上发生失电子发生氧化反应,正极上发生得电子的还原反应,Al-空气燃料电池以NaCl溶液为电解质溶液,正极上氧气得到电子;以KOH溶液为电解质溶液,电池反应为Al、氧气、KOH反应生成偏铝酸钾和水.
解答 解:Al-空气燃料电池以NaCl溶液为电解质溶液,正极上氧气得到电子,正极反应为O2+2H2O+4e-=4OH-;以KOH溶液为电解质溶液,电池反应为Al、氧气、KOH反应生成偏铝酸钾和水,该电池反应为4Al+3O2+4KOH=4KAlO2+2H2O,
故答案为:O2+2H2O+4e-=4OH-;4Al+3O2+4KOH=4KAlO2+2H2O.
点评 本题考查了化学电源新型电池,根据得失电子确定正极上通入氧气,难点是电极反应式的书写,注意碱性条件下铝失电子生成偏铝酸根离子,为易错点,题目难度不大.

练习册系列答案
相关题目
12.关于铯及其化合物的以下各说法中不正确的是( )
| A. | 氢氧化铯是一种强碱,比KOH的碱性强 | |
| B. | 铯与水或酸溶液反应剧烈,都生成氢气 | |
| C. | Cs的还原性比Na强,故Na+的氧化性大于Cs+ | |
| D. | Al的金属性大于Cs的金属性 |
9.下列各组物质中,不能按图示关系一步完成转化的是( )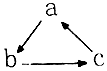

| A | B | C | D | |
| a | CO2 | Al(OH)3 | H2SO4 | HNO3 |
| b | Na2CO3 | NaAlO2 | SO2 | NO |
| c | NaHCO3 | Al2O3 | SO3 | NO2 |
| A. | A | B. | B | C. | C | D. | D |
13.下列分类或归类正确的是:①铝热剂、纯净矿泉水、冰水混合物均为混合物②NaOH、HD、IBr均为化合物③明矾、烧碱、硫酸均为强电解质④C60、金刚石、石墨均为碳的同素异形体⑤碘酒、淀粉溶液、水雾、纳米材料均为胶体( )
| A. | ①③⑤ | B. | ③④ | C. | ②④⑤ | D. | ③④⑤ |
8.3,3-二甲基-1-丁烯与氢气加成后得到的物质是( )
| A. | 2,2-二甲基-3-丁烷 | B. | 2,2-二甲基-2-丁烯 | ||
| C. | 2,2-二甲基-1-丁烯 | D. | 2,2-二甲基丁烷 |
8.下列物质中,化学式能真正表示该物质分子组成的是( )
| A. | Na2O | B. | SiO2 | C. | KOH | D. | H2SO4 |