题目内容
下列氧化还原反应中电子转移方向和数目不正确的是( )
A、 |
B、 |
C、 |
D、 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:氧化还原反应中失电子的元素化合价升高,得电子的元素化合价降低,化合价降低数目=化合价升高数目=转移的电子数目.
解答:
解:A.反应中Mn元素化合价由+4价降低都+2价,Cl元素化合价由-1价升高到0价,转移电子数为2,转移电子数=化合价降低总数目=化合价升高总数目,故A正确;
B.反应中Cu元素化合价由0价升高到+2价,N元素化合价由+5价降低到+4价,转移电子数为2,转移电子数=化合价降低总数目=化合价升高总数目,故B正确;
C.只有N元素化合价发生变化,N元素化合价分别由-3价、+5价变化为0价,转移电子数为15,故C正确;
D.Cl元素化合价分别由+5价、-1价变化为0价,转移电子数为5,故D错误.
故选D.
B.反应中Cu元素化合价由0价升高到+2价,N元素化合价由+5价降低到+4价,转移电子数为2,转移电子数=化合价降低总数目=化合价升高总数目,故B正确;
C.只有N元素化合价发生变化,N元素化合价分别由-3价、+5价变化为0价,转移电子数为15,故C正确;
D.Cl元素化合价分别由+5价、-1价变化为0价,转移电子数为5,故D错误.
故选D.
点评:本题考查了电子转移方向和数目,根据元素化合价变化来分析解答,易错选项是D,该反应中部分HCl不参加氧化还原反应,为易错点.

练习册系列答案
相关题目
下列物质在水溶液中发生电离,其电离方程式正确的是( )
| A、Ca(HCO3)2═Ca2++2HCO3- | ||
| B、KHSO4=K++HSO4- | ||
C、Na2SO4═2Na++SO
| ||
| D、BaCl2=Ba2++Cl2- |
在理论上不能用于设计原电池的化学反应是( )
| A、Al(OH)3(s)+NaOH(aq)═NaAlO2(aq)+2H2O(l)△H<0 |
| B、CH3CH2OH(l)+3O2(g)═2CO2(g)+3H2O(l)△H<0 |
| C、4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)△H<0 |
| D、H2(g)+Cl2(g)═2HCl(g)△H<0 |
下列说法正确的是( )
| A、c(H+)=0.1mol/L的甲酸溶液中,HCOO-和H+ 数目之和为0.1 NA |
| B、通常情况下,溴是液态,碘是固态,所以I-I键比Br-Br弱 |
| C、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,2C(NH4+)=C(SO42-) |
D、合成顺丁橡胶(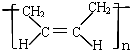 )的单体是CH2=CH-CH=CH2 )的单体是CH2=CH-CH=CH2 |
下列有关氧化还原反应的叙述中正确的是( )
| A、化合反应都不是氧化还原反应 |
| B、氧化还原反应的本质是元素化合价的升降 |
| C、失电子的反应物在反应中作氧化剂,反应中被还原 |
| D、金属单质在化学反应中一定做还原剂 |


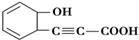 ,它与HBr气体1:1加成的产物可能有
,它与HBr气体1:1加成的产物可能有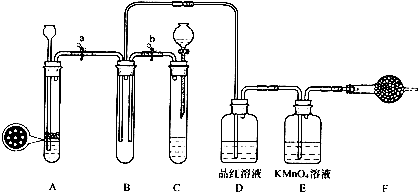
 有A、B、C、D、E五种元素(A、B、C、D、E分别代表元素符号),其中A元素原子核内只有一个质子;B元素的基态原子s亚层的总电子数比p亚层的总电子数多1;C元素的原子最外层电子数是次外层电子数的3倍;D位于B的下一周期,在同周期元素形成的简单离子中,D形成的简单离子半径最小;E的基态原子中电子排布在三个能级上,且这三个能级所含电子数均相同.
有A、B、C、D、E五种元素(A、B、C、D、E分别代表元素符号),其中A元素原子核内只有一个质子;B元素的基态原子s亚层的总电子数比p亚层的总电子数多1;C元素的原子最外层电子数是次外层电子数的3倍;D位于B的下一周期,在同周期元素形成的简单离子中,D形成的简单离子半径最小;E的基态原子中电子排布在三个能级上,且这三个能级所含电子数均相同.