题目内容
A~F均为中学化学中常见的物质,它们之间相互转化的关系如图所示(产物水等略去)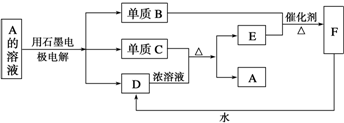
(1)写出下列物质的化学式:A ,D ,F .
(2)C和D的稀溶液不反应,但若B与C反应后再与D反应可生成A,试写出C和D的浓溶液反应化学方程式: .
(3)写出A的溶液电解时反应的化学方程式: .

(1)写出下列物质的化学式:A
(2)C和D的稀溶液不反应,但若B与C反应后再与D反应可生成A,试写出C和D的浓溶液反应化学方程式:
(3)写出A的溶液电解时反应的化学方程式:
考点:无机物的推断
专题:推断题
分析:电解A溶液得到三种物质,应是电解水及A,且有两种单质生成,则D为碱或酸,且单质C能与D浓溶液反应得到A,D不能为碱,只能为酸,可推知B为氧气、C为Cu、D为硫酸,E为二氧化硫,F为三氧化硫,A为硫酸铜,据此解答.
解答:
解:电解A溶液得到三种物质,应是电解水及A,且有两种单质生成,则D为碱或酸,且单质C能与D浓溶液反应得到A,D不能为碱,只能为酸,可推知B为氧气、C为Cu、D为硫酸,E为二氧化硫,F为三氧化硫,A为硫酸铜,
(1)由上述分析可知,A为CuSO4,D为H2SO4,F为SO3,故答案为:CuSO4;H2SO4;SO3;
(2)C和D的浓溶液反应化学方程式为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
(3)电解硫酸铜溶液时反应的化学方程式为:2CuSO4+2H2O
2H2SO4+2Cu+O2↑,故答案为:2CuSO4+2H2O
2H2SO4+2Cu+O2↑.
(1)由上述分析可知,A为CuSO4,D为H2SO4,F为SO3,故答案为:CuSO4;H2SO4;SO3;
(2)C和D的浓溶液反应化学方程式为:Cu+2H2SO4(浓)
| ||
| ||
(3)电解硫酸铜溶液时反应的化学方程式为:2CuSO4+2H2O
| ||
| ||
点评:本题考查无机物推断,涉及电解原理、硫元素化合物性质,难度中等,注意根据电解产物作为突破口推断.

练习册系列答案
相关题目
已知0.1mol/L H2A、NaHA溶液的pH分别为3.5、8.5,现有下列6种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①Na2A与HCl;②NaHA与NaOH;③NaOH与NH4Cl;④Na2A与NaHA;⑤Na2A与NaOH;⑥NaHA与HCl.下列各项排序正确的是( )
| A、pH:⑤>③>④>②>①>⑥ |
| B、c(A2-):⑤>②>④>①>⑥>③ |
| C、溶液中c(H+):⑥>①>④>②>③>⑤ |
| D、c(H2A):⑥>④>①>②>⑤>③ |
某同学用50mL 0.50mol?L-1的盐酸与50mL0.55mol?L-1的氢氧化钠溶液进行中和反应并计算中和热.造成测得的结果偏高的原因可能是( )
| A、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓 |
| B、做本实验的当天室温较高 |
| C、将50mL 0.55mol?L-1的氢氧化钠溶液取成了50mL 0.55mol?L-1的氨水 |
| D、在量取盐酸时仰视读数 |
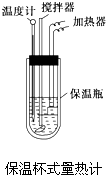 在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.