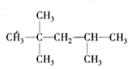
题目内容
2.下列图象与选项对应的是( )| A. | 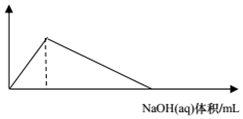 AlCl3(aq)中滴入NaOH(aq) | B. | 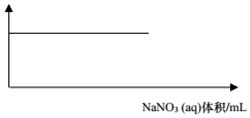 Al(OH)3中滴入NaNO3(aq) | ||
| C. | 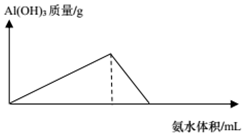 AlCl3(aq)中滴入氨水 | D. | 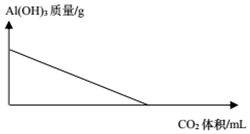 Al(OH)3中通入CO2 |
分析 A.氢氧化钠再和氯化铝反应生成氢氧化铝沉淀,当氢氧化钠过量时,氢氧化钠再和氢氧化铝反应生成可溶性的偏铝酸钠;
B.氢氧化铝沉淀和强酸强碱盐硝酸钠不反应;
C.氢氧化铝不溶于弱碱,在AlCl3溶液中滴加氨水至过量,逐渐产生沉淀,且沉淀不溶解;
D.Al(OH)3不溶于弱酸碳酸.
解答 解:A.AlCl3(aq)中滴入NaOH(aq)先发生:AlCl3+3NaOH═Al(OH)3↓+3NaCl,当氢氧化钠过量时,Al(OH)3+NaOH═NaAlO2+2H2O,形成氢氧化铝沉淀的氢氧化钠与溶解氢氧化铝的氢氧化钠的物质的量之比为3:1,与图象不符,故A错误;
B.氢氧化铝为两性物质,能溶于强酸强碱溶液,但硝酸钠为强酸强碱盐,溶液呈中性,所以两者不反应,即沉淀不溶解,与图象相符,故B正确;
C.在AlCl3溶液中滴加氨水至过量:AlCl3+3NH3•H2O=Al(OH)3↓+3NH4Cl,逐渐产生沉淀,且沉淀不溶解,与图象不符,故C错误;
D.CO2溶于水生成弱酸碳酸,Al(OH)3不溶于弱酸碳酸,Al(OH)3中通入CO2,无沉淀生成,与图象不符,故D错误;
故选B.
点评 本题考查了氯化铝、氢氧化铝的性质,掌握氢氧化铝的两性以及知道铝离子完全转化为沉淀和沉淀完全溶解时两部分氢氧化钠物质的量的关系是解答关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.己知C5H11N的同分异构体中含有苯坏的有很多种(不考虑立体异构),其中苯环上有一个侧链、二个侧链和三个侧链的种数分别是( )
| A. | 5、9、6 | B. | 4、6、6 | C. | 3、9、7 | D. | 4、6、7 |
13.下列有关说法正确的是( )
| A. | 实验室制氢气,为了加快反应速率,可向稀硫酸中滴加少量硝酸铜溶液 | |
| B. | 可用勒夏特列原理解释2NO2(g)?N2O4(g)体系加压后颜色变深 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0可通过加压方式增大其平衡常数 | |
| D. | 二氧化硫和乙烯两种气体分别通入Br2的CCl4溶液,能使溶液褪色的是乙烯气体 |
10.X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列说法正确的是( )
| A. | 由mXa-与nYb-得,m+b=n+a | |
| B. | X2-的还原性一定大于Y- | |
| C. | X、Y一定是同周期元素 | |
| D. | 若X的原子半径大于Y,则X的氢化物稳定性一定大于Y的氢化物 |
17.可检验FeC13溶液中是否含FeCl2的试剂是( )
| A. | KSCN溶液 | B. | 氯水 | C. | NaOH溶液 | D. | 酸性KMnO4溶液 |
7.向含有下列离子的各组溶液中分别通入足量相应气体,各离子还能大量存在的是( )
| A. | Fe3+、SO42-,通氨气 | B. | Na+、HCO3-,通氯气 | ||
| C. | Fe2+、NO3-,通氯化氢 | D. | Ca2+、Br-,通二氧化硫 |
14.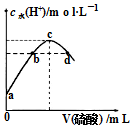 常温下,向20mL0.1mol•L-1氨水中滴加某浓度的硫酸溶液,溶液中水电离的氢离子浓度随加入硫酸的体积变化如图.下列说法错误的是( )
常温下,向20mL0.1mol•L-1氨水中滴加某浓度的硫酸溶液,溶液中水电离的氢离子浓度随加入硫酸的体积变化如图.下列说法错误的是( )
 常温下,向20mL0.1mol•L-1氨水中滴加某浓度的硫酸溶液,溶液中水电离的氢离子浓度随加入硫酸的体积变化如图.下列说法错误的是( )
常温下,向20mL0.1mol•L-1氨水中滴加某浓度的硫酸溶液,溶液中水电离的氢离子浓度随加入硫酸的体积变化如图.下列说法错误的是( )| A. | 若a等于1.0×10-11 mol•L-1,则此时氨水的电离度为1% | |
| B. | c点时氨水与硫酸恰好完全反应 | |
| C. | c点所示溶液中:c(H+)-c(OH-)═c(NH3•H2O) | |
| D. | 若b、d对应的水电离的氢离子浓度为1.0×10-7 mol•L-1,此时两溶液中都存在:c(NH4+)═2c(SO42-) |
11.下列生活中常用的食物储存方法中,所加物质不与氧气反应的是( )
| A. | B. | C. | D. |
 |  |  |  |
| 用浸泡过KMnO4溶液的纸张保鲜水果 | 食用油中添加 TBHQ(一种酚类物质) | 红酒中添加 一定量的SO2 | 食品包装袋中 放置还原铁粉 |
| A. | A | B. | B | C. | C | D. | D |
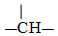 、
、 等结合而成的.试写出同时满足下列条件的烷烃的结构简式:
等结合而成的.试写出同时满足下列条件的烷烃的结构简式: