题目内容
7.8克某常见的烃完全燃烧后生成的气体通入足量的石灰水,得到60克沉淀,测得在同温、同压、同体积时该烃的质量是H2质量的13倍,请通过计算写出它的结构简式.
考点:有关有机物分子式确定的计算
专题:有机物分子组成通式的应用规律
分析:测得在同温、同压、同体积时该烃的质量是H2质量的13倍,根据m=nM可知,该烃的摩尔质量为氢气的13倍,据此可以计算出该烃的摩尔质量,然后计算出7.8g该烃的物质的量;通入足量石灰水生成的沉淀为碳酸钙,根据碳酸钙的质量可以计算出碳酸钙的物质的量,根据C原子守恒计算出该烃中含有的C原子数,再根据该烃的摩尔质量计算出该烃的分子式,根据分子式确定结构简式.
解答:
解:7.8该烃完全燃烧后生成的气体通入足量的石灰水,得到60克沉淀,沉淀为碳酸钙,其物质的量为:
=0.6mol,根据质量守恒,7.8g该烃中含有C的物质的量为0.6mol;
在同温、同压、同体积的气体具有相同的物质的量,根据m=nM可知,该烃的摩尔质量是H2质量的13倍,该烃的摩尔质量为:2g/mol×13=26g/mol,
7.8g该烃的物质的量为:n=
=0.3mol,
该烃中含有碳原子数为:
=2,
由于该烃的相对分子量为26,则该烃分子中含有H的数目为:
=2,
该烃的分子式为:C2H2,为乙炔,其结构简式为:CH≡CH,
答:该烃的结构简式为CH≡CH.
| 60g |
| 100g/mol |
在同温、同压、同体积的气体具有相同的物质的量,根据m=nM可知,该烃的摩尔质量是H2质量的13倍,该烃的摩尔质量为:2g/mol×13=26g/mol,
7.8g该烃的物质的量为:n=
| 7.8g |
| 26g/mol |
该烃中含有碳原子数为:
| 0.6mol |
| 0.3mol |
由于该烃的相对分子量为26,则该烃分子中含有H的数目为:
| 26-12×2 |
| 1 |
该烃的分子式为:C2H2,为乙炔,其结构简式为:CH≡CH,
答:该烃的结构简式为CH≡CH.
点评:本题考查了有机物分子式、结构简式的确定,题目难度不大,注意掌握常见有机物结构与性质,能够根据质量守恒、烃的燃烧通式计算有机物的分子式、结构简式,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
下列实验方案设计合理且能达到相应实验预期目的是( )
A、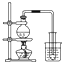 制取少量蒸馏水 |
B、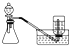 用铜和浓硝酸制取少量NO2 |
C、 证明氧化性:Cl2>Br2>I2 |
D、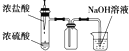 制取HCl且除去多余的气体 |
金属钠通常保存在( )
| A、水中 | B、煤油中 |
| C、汽油中 | D、四氯化碳中 |
钢铁在很弱的酸性或中性条件下发生电化学腐蚀时,正极的反应式为( )
| A、Fe-2e-═Fe2+ |
| B、2H++2e-═H2↑ |
| C、2H2O+O2+4e-═4OH- |
| D、Fe-3e-═Fe3+ |

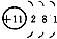
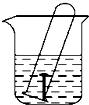 按如图所示进行铁腐蚀的实验,一周后观察:
按如图所示进行铁腐蚀的实验,一周后观察: