题目内容
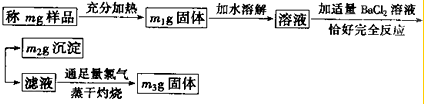
实验室需要纯净的氯化钾,现有氯化钾中含有少量溴化钾、硫酸钾和氯化铵.按照如图所示实验方案提纯分离出氯化钾:
列式计算该氯化钾样品中氯化铵、硫酸钾和溴化钾的质量分数.
其中氯化铵加热可分NH4Cl
NH3↑+HCl↑
氯气通入溴化钾溶液:Cl2+2KBr═2KCl+Br2.
列式计算该氯化钾样品中氯化铵、硫酸钾和溴化钾的质量分数.

其中氯化铵加热可分NH4Cl
| ||
氯气通入溴化钾溶液:Cl2+2KBr═2KCl+Br2.
由图及物质的性质可知,充分加热时NH4Cl分解,则(m-m1)g为NH4Cl的质量,m2g为BaSO4的质量,由硫酸根离子守恒可计算硫酸钾的质量,m3g为KCl的质量,KCl来源于硫酸钾与氯化钡的反应生成及Cl2+2KBr═2KCl+Br2中反应生成,
则氯化铵的质量分数为
×100%=
%,
硫酸钾的质量分数为
×100%=
%,
溴化钾的质量为[m1g-m2g×
-(m3g-m2g×
)]×
,
则溴化钾的质量分数为
%,
答:氯化钾样品中氯化铵、硫酸钾和溴化钾的质量分数分别为
%、
%、
%.
则氯化铵的质量分数为
| (m-m1)g |
| mg |
| 100(m-m1) |
| mg |
硫酸钾的质量分数为
(m2g×
| ||
| mg |
100(m2×
| ||
| m |
溴化钾的质量为[m1g-m2g×
| 174 |
| 233 |
| 149 |
| 233 |
| 238 |
| 149 |
则溴化钾的质量分数为
100(m1-
| ||||
| m |
答:氯化钾样品中氯化铵、硫酸钾和溴化钾的质量分数分别为
| 100(m-m1) |
| mg |
100(m2×
| ||
| m |
100(m1-
| ||||
| m |

练习册系列答案
相关题目
工业制备氯化铜时,常将浓盐酸用蒸汽加热到80℃左右,慢慢加入粗CuO粉末(含有杂质![]() 、
、![]() )充分反映,使之溶解,得到强酸性的混合溶液,欲从该混合溶液中制备纯净的
)充分反映,使之溶解,得到强酸性的混合溶液,欲从该混合溶液中制备纯净的![]() 溶液。请参照下表给出的数据回答下列问题:
溶液。请参照下表给出的数据回答下列问题:
| 部分金属阳离子 |
|
|
|
| 以氢氧化物形式沉淀完全是的pH | ≥9.6 | ≥3.7 | ≥6.4 |
(1)第一步除去![]() ,能否直接调整pH=9.6将
,能否直接调整pH=9.6将![]() 转化为沉淀出去 (填“能”或“否”);理由是 。
转化为沉淀出去 (填“能”或“否”);理由是 。
若用强氧化剂![]() 将
将![]() 氧化为
氧化为![]() ,则加入
,则加入![]() 后,溶液的pH的变化是 。
后,溶液的pH的变化是 。
A.一定增大 B.一定减小 C.可能增大 D.可能减小
(2)除去溶液中的![]() 的方法是调整溶液的pH=3.7,现有下列试剂均可使强酸性溶液的pH调整到3.7,可选用的有 。
的方法是调整溶液的pH=3.7,现有下列试剂均可使强酸性溶液的pH调整到3.7,可选用的有 。
A.![]() B.氨水 C.
B.氨水 C.![]() D.
D.![]() E.
E.![]() F.
F.![]()
(3)亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液,那么保存亚铁盐溶液时应该如何防止亚铁盐氧化?
