题目内容
教材显示地球上99%的溴元素存在于海洋中,且海水中Br-的含量一般为0.067g?L-1.从海水中提取溴的工业流程如下:

(1)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用到溴的性质是 .
(2)上述流程中吹出的溴蒸气,也可以用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的化学方程式: .
(3)以上步骤I中已获得游离态的溴,步骤Ⅱ又将之转化成化合态的溴,其目的是 .
(4)实验室从溴水中分离溴还可以用萃取法,下列不可用作溴的萃取剂的是 .
a.乙酸 b.四氯化碳 c.酒精 d.苯.

(1)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用到溴的性质是
(2)上述流程中吹出的溴蒸气,也可以用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的化学方程式:
(3)以上步骤I中已获得游离态的溴,步骤Ⅱ又将之转化成化合态的溴,其目的是
(4)实验室从溴水中分离溴还可以用萃取法,下列不可用作溴的萃取剂的是
a.乙酸 b.四氯化碳 c.酒精 d.苯.
考点:海水资源及其综合利用
专题:元素及其化合物
分析:流程分析可知海水通过一定方法淡化得到淡水和卤水,卤水加入氧化剂氧化溴离子为单质溴,通入热空气或水蒸气吹出Br2,利用的是溴单质的易挥发性,再利用酸溶液中溴酸根离子和溴离子发生氧化还原反应得到溴单质;
(1)溴单质具有易挥发性;
(2)溴与二氧化硫水溶液反应生成硫酸和溴化氢;
(3)过程中得到溴单质,通过热空气吹出后用纯碱吸收得到溴酸根和溴离子,在酸溶液中重新得到溴单质;
(4)依据萃取的原则是萃取剂不溶于水,在水溶液中分层;
(1)溴单质具有易挥发性;
(2)溴与二氧化硫水溶液反应生成硫酸和溴化氢;
(3)过程中得到溴单质,通过热空气吹出后用纯碱吸收得到溴酸根和溴离子,在酸溶液中重新得到溴单质;
(4)依据萃取的原则是萃取剂不溶于水,在水溶液中分层;
解答:
解:(1)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用到溴的性质是易挥发;
故答案为:挥发性;
(2)上述流程中吹出的溴蒸气,也可以用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.溴与二氧化硫水溶液反应生成硫酸和溴化氢,反应的化学方程式为:
Br2+SO2+2H2O=2HBr+H2SO4;
故答案为:Br2+SO2+2H2O=2HBr+H2SO4;
(3)步骤I中溴单质的浓度低,若直接蒸馏,生产成本高;经步骤Ⅱ、Ⅲ,实际上是将溴水浓缩,使溴元素的富集;
故答案为:溴元素的富集;
(4)实验室从溴水中分离溴还可以用萃取法,下列不可用作溴的萃取剂的是和水溶液互溶的试剂;
a.乙酸乙溶于水,不能做萃取剂,故a错误;
b.四氯化碳不溶于水,可以萃取溴单质,故b正确;
c.酒精极易溶于水,不能分层,不能做萃取剂,故c错误;
d.苯是不溶于水比水轻的试剂,可以做萃取溴单质的萃取剂,故d正确;
故答案为:ac;
故答案为:挥发性;
(2)上述流程中吹出的溴蒸气,也可以用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.溴与二氧化硫水溶液反应生成硫酸和溴化氢,反应的化学方程式为:
Br2+SO2+2H2O=2HBr+H2SO4;
故答案为:Br2+SO2+2H2O=2HBr+H2SO4;
(3)步骤I中溴单质的浓度低,若直接蒸馏,生产成本高;经步骤Ⅱ、Ⅲ,实际上是将溴水浓缩,使溴元素的富集;
故答案为:溴元素的富集;
(4)实验室从溴水中分离溴还可以用萃取法,下列不可用作溴的萃取剂的是和水溶液互溶的试剂;
a.乙酸乙溶于水,不能做萃取剂,故a错误;
b.四氯化碳不溶于水,可以萃取溴单质,故b正确;
c.酒精极易溶于水,不能分层,不能做萃取剂,故c错误;
d.苯是不溶于水比水轻的试剂,可以做萃取溴单质的萃取剂,故d正确;
故答案为:ac;
点评:本题考查了海水资源的利用分析判断,主要是流程操作的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
X和Y属短周期元素,X原子的次外层电子数是最外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,则X和Y所形成的化合物的化学式可表示为( )
| A、XY |
| B、XY2 |
| C、XY3 |
| D、XY4 |
利用某有机物之间的转换可以贮存太阳能,如降冰片二烯(NBD)经太阳光照可转化成四环烷(Q),其反应式可表示为: △H=+88.62kJ/mol
△H=+88.62kJ/mol
下列有关说法不正确的是( )
 △H=+88.62kJ/mol
△H=+88.62kJ/mol下列有关说法不正确的是( )
| A、一定条件下,1mol NBD最多可与2 mol Br2发生加成反应 |
| B、物质Q的能量比NBD的低 |
| C、物质Q的一氯取代物只有3种 |
| D、NBD和Q二者互为同分异构体 |
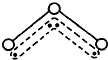 O3能吸收有害紫外线,保护人类赖以生存的空间.O3分子的结构如图,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答:
O3能吸收有害紫外线,保护人类赖以生存的空间.O3分子的结构如图,呈V型,键角116.5℃.三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键--三个O原子均等地享有这4个电子.请回答: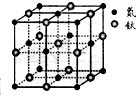 现有5种短周期元素A、B、C、D、E,原子序数依次增大.A的同位素中有一种核素无中子,B最外层上电子数是次外层电子数的两倍,C元素最简单的氢化物Y的水溶液呈碱性,E是短周期中电负性最小的元素.D与可与A、B、C、E四种元素分别形成原子个数比不相同的常见化合物.回答下列问题:
现有5种短周期元素A、B、C、D、E,原子序数依次增大.A的同位素中有一种核素无中子,B最外层上电子数是次外层电子数的两倍,C元素最简单的氢化物Y的水溶液呈碱性,E是短周期中电负性最小的元素.D与可与A、B、C、E四种元素分别形成原子个数比不相同的常见化合物.回答下列问题: