题目内容
下列有关原电池的叙述中,错误的是( )
| A、原电池是将化学能转化为电能的装置 |
| B、用导线连接的两种不同金属同时插入液体中,能形成原电池 |
| C、在原电池中,电子流出的一极是负极,发生氧化反应 |
| D、在原电池放电时,电解质溶液中的阳离子向正极移动 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.原电池是将化学能转化为电能的装置;
B.根据原电池的构成条件分析;
C.负极失电子发生氧化反应;
D.溶液中阳离子向正极移动.
B.根据原电池的构成条件分析;
C.负极失电子发生氧化反应;
D.溶液中阳离子向正极移动.
解答:
解:A.原电池反应中能自发的进行氧化还原反应,是将化学能转化为电能的装置,故A正确;
B.原电池的构成条件①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,若用导线连接的两种不同金属同时插入酒精中,则不能形成原电池,故B错误;
C.原电池中,负极失电子发生氧化反应,则电子流出的一极是负极,故C正确;
D.原电池中,电解质溶液中的阳离子向正极移动,阴离子向负极移动,故D正确;
故选B.
B.原电池的构成条件①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,若用导线连接的两种不同金属同时插入酒精中,则不能形成原电池,故B错误;
C.原电池中,负极失电子发生氧化反应,则电子流出的一极是负极,故C正确;
D.原电池中,电解质溶液中的阳离子向正极移动,阴离子向负极移动,故D正确;
故选B.
点评:本题考查的内容是高考中的常见考点,属于基础性试题的考查,难度不大,明确原电池的工作原理、构成条件是答题的关键.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
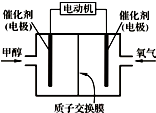 甲醇(CH3OH)燃料电池可用作电动汽车电源,如图为电池示意图.在电池的一极通入甲醇,另一极通入氧气,工作时H+由负极移向正极.下列叙述不正确的是( )
甲醇(CH3OH)燃料电池可用作电动汽车电源,如图为电池示意图.在电池的一极通入甲醇,另一极通入氧气,工作时H+由负极移向正极.下列叙述不正确的是( )| A、外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g |
| B、通甲醇一端为负极 |
| C、正极反应为:O2+4H++4e-=2H2O |
| D、负极反应为:CH3OH+H2O+6e-=CO2↑+6H+ |
下列离子方程式中正确的是( )
| A、某钾盐K2A 的水溶液显碱性,其原因是:A2-+2H2O?H2A+2OH- | ||||||
| B、在30mL 1mol?L-1的Na2SO3溶液中通入标准状况下的Cl2 224mL:H2O+3SO32-+Cl2═SO42-+2HSO3-+2Cl- | ||||||
C、碳酸氢铵溶液与足量的NaOH溶液混合加热:NH
| ||||||
D、在Ba(HCO3)2溶液中逐滴滴入NaHSO4 溶液至Ba2+恰好完全沉淀时:Ba2++2HCO
|
下列关于溶液和胶体的叙述,正确的是( )
| A、一束光线分别通过溶液和胶体时,后者能看到一条光亮的“通路”,前者则没有 |
| B、溶液是电中性的,胶体是带电的 |
| C、溶液中溶质分子可以通过滤纸,胶体中分散质粒子则不能通过滤纸 |
| D、通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 |
下列溶液中的氯离子浓度与50mL0.1mol/L氯化铝溶液中的氯离子浓度相等的是( )
| A、150mL 0.1mol/L NaCl |
| B、75mL 0.2mol/L NH4Cl |
| C、100mL 0.3mol/L KCl |
| D、150mL 0.1mol/L FeCl3 |
硒(Se)是人体必需的一种微量元素,其单质可用于制光敏电阻、复印机的硒鼓等等.工业上提取硒的方法之一是用硫酸和硝酸钠处理含硒的工业废料,得到亚硒酸(H2SeO3)和少量硒酸(H2SeO4),富集后再将它们与盐酸共热,将H2SeO4转化为H2SeO3,主要反应为2HCl+H2SeO4═H2SeO3+H2O+Cl2↑,然后向溶液中通入SO2将硒元素还原为单质硒沉淀.据此正确的判断为( )
| A、H2SeO4的氧化性比Cl2弱 |
| B、SeO2的氧化性比SO2弱 |
| C、H2SeO4的氧化性比H2SeO3强 |
| D、析出1mol硒,需亚硒酸、SO2和水各1mol |
下列说法正确的是( )
| A、甲烷是最简单的烷烃,其含碳量最高 |
| B、烷烃完全燃烧时,生成CO2和H2O的物质的量相等 |
| C、烯烃的分子组成中,碳和氢的质量比固定不变,烯烃通式为CnH2n(n≥2) |
| D、烯烃完全燃烧时,生成CO2和H2O的物质的量不相等 |
 常温下,向10mL0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1醋酸溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,向10mL0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1醋酸溶液,所得滴定曲线如图所示.下列说法正确的是( )| A、pH=7时,所加醋酸溶液的体积为10mL |
| B、pH<7时,溶液中c(CH3COO-)>c(Na+) |
| C、7<pH<13时,溶液中c(Na+)+c(H+)>c(CH3COOH)+c(OH-) |
| D、继续滴加0.1 mol?L-1醋酸溶液,溶液pH可以变为1 |
标准状况下,112mL某气体的质量为0.14g,则其摩尔质量为( )
| A、28 g |
| B、14 g |
| C、14g/mol |
| D、28g/mol |