题目内容
M(NO3)2热分解化学方程式为:2M(NO3)2
2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下收集11200mL的气体,那么M的摩尔质量是
| ||
24g/mol
24g/mol
.分析:根据标准状况下的气体摩尔体积计算出气体的物质的量,再根据反应方程式中化学计量数关系计算出29.6g M(NO3)2的物质的量,根据M=
计算出摩尔质量,最后计算M的摩尔质量.
| m |
| n |
解答:解:在标准状况下收集11200mL的气体体积为11.2L,物质的量为:
mol=0.5mol,
根据反应方程式2M(NO3)2
2MO+4NO2↑+O2↑,
2 4 1
硝酸盐的物质的量为:0.5mol×
=0.2mol,M(NO3)2的摩尔质量为:
=148g/mol,
摩尔质量在以g/mol为单位时,在数值上与相对分子量或相对原子量相等,所以M(NO3)2的式量为:148,M的相对原子量为:148-62×2=24,
所以M的摩尔质量为:24g/mol,
故答案为:24g/mol.
| 11.2 |
| 22.4 |
根据反应方程式2M(NO3)2
| ||
2 4 1
硝酸盐的物质的量为:0.5mol×
| 2 |
| 4+1 |
| 29.6g |
| 0.2mol |
摩尔质量在以g/mol为单位时,在数值上与相对分子量或相对原子量相等,所以M(NO3)2的式量为:148,M的相对原子量为:148-62×2=24,
所以M的摩尔质量为:24g/mol,
故答案为:24g/mol.
点评:本题考查了摩尔质量的计算,题目难度不大,要求熟练掌握物质的量与气体摩尔体积、摩尔质量之间的转化关系.

练习册系列答案
相关题目
M(NO3)2热分解的反应方程式为2M(NO3)2 2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下得到2.24L氧气,则M的摩尔质量是( )
2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下得到2.24L氧气,则M的摩尔质量是( )
| A.24 g/mol | B.24 | C.64 g/mol | D.64 |
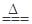 2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下得到2.24L氧气,则M的摩尔质量是( )
2MO+4NO2↑+O2↑,加热29.6g M(NO3)2使其完全分解,在标准状况下得到2.24L氧气,则M的摩尔质量是( )