题目内容
用NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A、标准状况下,11.2L H2O所含的水分子数目为0.5NA |
| B、16g O2和O3的混合气体中所含的氧原子数目为NA |
| C、1.00mol/L Na2CO3溶液中所含Na+的数目为2NA |
| D、0.1mol Zn与含0.1mol HCl的盐酸充分反应,产生H2数目为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:本题根据阿伏伽德罗常数计算粒子的个数,在首先求出物质的量,然后乘以阿伏伽德罗常数可得;物质的量计算,对于气体,在标准状况下可以用气体体积除以标准摩尔体积,对于所有物质,都可以用质量除以摩尔计量求出.
解答:
解:A.水为液体,不能用标况下气体的摩尔体积来计算,故A错误;
B.氧气和臭氧的原子均为氧原子,故16g氧原子的物质的量为1mol,氧原子数目为NA ,故B正确;
C.没有指明碳酸钠的体积,故C错误;
D.锌与盐酸反应,盐酸不足,按盐酸的量来计算,产生H2数目为0.1NA,故D错误;
故选B.
B.氧气和臭氧的原子均为氧原子,故16g氧原子的物质的量为1mol,氧原子数目为NA ,故B正确;
C.没有指明碳酸钠的体积,故C错误;
D.锌与盐酸反应,盐酸不足,按盐酸的量来计算,产生H2数目为0.1NA,故D错误;
故选B.
点评:本题首先求出物质的量,然后乘以阿伏伽德罗常数就可以计算粒子的个数.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
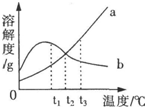 有关a、b两种物质的溶解度曲线如图所示,下列叙述不正确的是( )
有关a、b两种物质的溶解度曲线如图所示,下列叙述不正确的是( )| A、a物质的溶解度随着温度的升高而增大 |
| B、在t2℃时,a、b两种物质的溶液中溶质的质量分数一定相等 |
| C、t3℃时,a物质的溶解度大于b物质的溶解度 |
| D、将a、b两种物质的饱和溶液从t3℃降温至t1℃,a有晶体析出,b无晶体析出 |
某固体仅有一种元素组成,其密度为5g/cm3,用X射线研究该固体的结果表明,在边长为1nm(1nm=10-9m)的立方体中仅有20个原子,则此元素的相对原子质量接近( )
| A、32 | B、65 |
| C、120 | D、150 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、6.5g金属锌变成锌离子时失去的电子数目为0.1NA |
| B、常温常压下,2g氢气所含原子数目为2NA |
| C、标准状况下,11.2LH2O含有的分子数为0.5NA |
| D、常温常压下,11.2LCl2含有的分子数为0.5NA |
对于质量相同的H2SO4和H3PO4,下列说法正确的是( )
| A、所含氢原子数不相同 |
| B、所含氧原子数不相同 |
| C、所含硫原子数与磷原子数相同 |
| D、H2SO4体积与H3PO4体积相同 |
航天飞船常用铝粉与高氯酸铵(NH4ClO4)的混合物作为固体燃料,高氯酸铵中Cl元素的化合价是( )
| A、+1 | B、+3 | C、+5 | D、+7 |
下列各组物质在溶液中不发生化学反应而能共存的是( )
| A、MgCl2 AgNO3 KNO3 HCl |
| B、H2SO4 BaCl2 Na2SO4 NaOH |
| C、Na2SO4 KNO3 Na2CO3 NaCl |
| D、NH4HCO3 NaOH NaCl HCl |
NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、1molCH5+离子(碳正离子)所含电子数为10NA |
| B、含0.5molNa2SO4的溶液中含有NA个Na+ |
| C、1molNa2O2固体中含有2NA个O- |
| D、3.2克CH4气体完全燃烧需O2的分子数为0.2NA |