题目内容
15.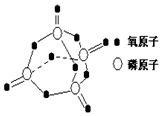 研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1 mol 化学键时所需吸收的能量.表是部分化学键的键能数据:
研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1 mol 化学键时所需吸收的能量.表是部分化学键的键能数据:| 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ•mol-1 | 197 | 360 | 499 | X |
分析 白磷燃烧的方程式为P4+5O2=P4O10,根据化学键的断裂和形成的数目进行计算,由此分析解答.
解答 解:白磷燃烧的方程式为P4+5O2=P4O10,1mol白磷完全燃烧需拆开6mol P-P、5mol O=O,形成12molP-O、4mol P=O,所以12mol×360kJ/mol+4mol×xkJ/mol-(6mol×197 kJ/mol+5 mol×499 kJ/mol)=2378.0kJ,解得x=433.75,故答案为:433.75.
点评 本题考查意热化学方程式的书写方法和计算应用,注意反应热的计算,特别是注意分析白磷的氧化磷的分子结构,正确判断共价键的类型和数目.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列化学用语表示正确的是( )
| A. | 小苏打电离方程式:NaHCO3═Na++H++CO32- | |
| B. | Cl-的结构示意图: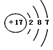 | |
| C. | H2O的电子式: | |
| D. | 乙烯的最简式:C2H4 |
6.已知塑化剂DEHP的分子式为C24H38O4,相对分子质量为390,沸点为386.9℃,下列有关说法不正确的是( )
| A. | 标准状况下,22.4LDEHP的物质的量为1mol | |
| B. | DEHP中碳原子与氧原子的数目之比为6:1 | |
| C. | 1molDEHP中约含有6.02×1023个分子 | |
| D. | DEHP的摩尔质量是350g/mol |
10.下列物质在水中的电离方程式错误的是( )
| A. | Fe2(SO4)3═2Fe3++3SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | Ca(OH)2═Ca2++2OH- | D. | NaHSO4═Na++H++SO42- |
20.某温度下,测得某医用钢瓶中有22.4LO2,下列叙述正确的是( )
| A. | 它的质量是32 g | B. | 约含有6.02×1023个O2分子 | ||
| C. | 含有2 mol O | D. | 红热的铁丝可在其中剧烈燃烧 |
7.
| 物质 | 分子数 | 质量(g) | 物质的量(mol) | 摩尔质量(g•mol-1) |
| N2 | 3.01×1023 | |||
| CO2 | 4.4 | |||
| HCl | 0.5 | |||
| H2SO4 | 49 |
4.利用反应:2NO(g)+2CO(g)?2CO2(g)+N2(g)△H=-746,8kJ•mol-1,可净化汽车尾气,如果要同时提高反应的速率和 NO 的转化率,采取的措施是( )
| A. | 降低温度 | |
| B. | 升高温度同时充入N2 | |
| C. | 增大压强 | |
| D. | 及时将 CO2和 N2 从反应体系中移走 |
5.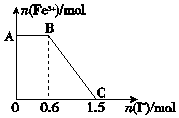 已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
 已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )| A. | 图中AB段的氧化剂为K2Cr2O7 | |
| B. | 图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 | |
| C. | 开始加入的K2Cr2O7为0.15 mol | |
| D. | K2Cr2O7与FeSO4反应的物质的量之比为1:6 |