题目内容
6.汽车尾气排放的一氧化碳、氮氧化物等气体已成为大气污染的主要来源.根据下列示意图1回答有关问题: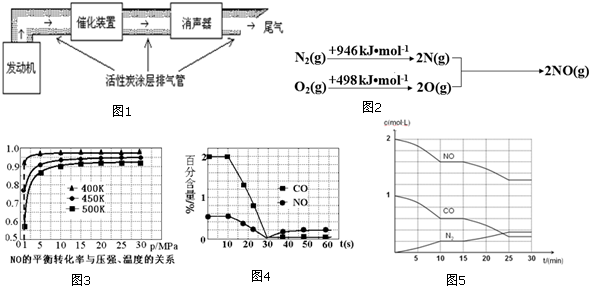
(一)汽车发动机工作时会引发N2(g)+O2(g)=2NO(g)△H=+180kJ•mol-1,其能量变化示意图2如:
则NO中氮氧键的键能为632kJ•mol-1.
(二)催化装置中涉及的反应之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0.
(1)①探究上述反应中NO的平衡转化率与压强、温度的关系,得到图3所示的曲线.催化装置比较适合的温度和压强是400K,1MPa.
②测试某型号汽车在冷启动(冷启动指发动机水温低的情况下启动)时催化装置内CO和NO百分含量随时间变化曲线如图4所示.则前10s 内,CO和NO百分含量没明显变化的原因是尚未达到催化剂工作温度(或尚未达到反应的温度).
(2)为了模拟催化转化器的工作原理,在t℃时,将2molNO与1mol CO充入1L反应容器中,反应过程中NO(g)、CO(g)、N2(g)的物质的量浓度变化如图5所示,
①则反应进行到10min时,NO的平均反应速率为0.04mol•L-1•min-1.
②15min~25min内NO、CO、N2的浓度发生了变化,引起该变化的条件是降低温度.③当25min达到平衡后,若保持体系温度为t℃,再向容器中充入NO、N2气体各1mol,平衡将向左移动(填“向左”、“向右”或“不”).
(三)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)?N2(g)+xCO2(g)△H=-bkJ•mol-1.若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是AD.
A.增加排气管长度 B.增大尾气排放口
C.升高排气管温度 D.添加合适的催化剂.
分析 (一)△H=反应物的键能总和-生成物的键能总和;
(二)(1)①综合考虑NO的转化率和成本;
②汽车冷启动时的尾气催化处理CO、NO百分含量随时间变化曲线变化分析,开始的气体含量变化不大,说明温度低,催化剂的作用未起作用;
(2)①根据V=$\frac{△n}{\frac{V}{△t}}$来计算;
②根据氮气的变化来确定NO、CO的变化;结合图象根据外界条件对化学平衡的影响来判断;
③再向容器中充入NO、N2气体各1mol,分母增加的幅度大,导致QC减小由此确定平衡移动方向;
(三)A.增加排气管长度,增大了相当于增大了固体的接触面积,加快了化学反应速率,对平衡无影响;
B.增大尾气排放口,对反应速率和平衡不产生影响;
C.升高排气管温度,温度升高,平衡左移,不利于NOx转化;
D.添加合适的催化剂,加快化学反应速率,对平衡无影响.
解答 解:(一)设NO中氮氧键的键能为x,△H=反应物的键能总和-生成物的键能总和=(946+498)kJ•mol-1-2×x=180kJ•mol-1,解得x=632 kJ•mol-1,
故答案为:632;
(二)(1)①由图2可知,等压条件下,温度越低,NO的转化率越高,因此温度选400K,同温下,NO的转化率随着温度的升高变化不大,所以选用较为经济的1MPa,
故答案为:400K,1MPa:
②汽车冷启动时的尾气催化处理CO、NO百分含量随时间变化曲线变化分析,开始的气体含量变化不大,说明温度低,催化剂的作用未起作用;证明反应未达到催化剂工作温度(或尚未达到反应的温度);
故答案为:尚未达到催化剂工作温度(或尚未达到反应的温度);
(2)①由图象可知在10min内NO的物质的量变化0.4mol,则NO的平均反应速率为=$\frac{0.4}{\frac{1}{10}}$mol•L-1•min-1=0.04mol•L-1•min-1,
故答案为:0.04mol•L-1•min-1;
②由图象可知,15min~25min内NO、CO浓度在减少,N2的浓度在增加,平衡向正反应方向移动,降低温度,平衡向正反应方向移动,
故答案为:降低温度;
③化学平衡常数等于平衡时生成物的浓度幂之积比上反应物浓度幂之积,所以K=$\frac{{C}^{2}(C{O}_{2})•C({N}_{2})}{{C}^{2}(NO)•{C}^{2}(CO)}$,由平衡常数表达式可知一氧化氮的系数是2次方,所以再向容器中充入NO、N2气体各1mol,分母增加的幅度大,导致QC减小,即平衡逆向移动,即向左移动,
故答案为:向左;
(三)xC(s)+2NOx(g)?N2(g)+xCO2 (g)△H=-b kJ•mol-1.此反应为放热反应,
A.增加排气管长度,增大了相当于增大了固体的接触面积,加快了化学反应速率,故A正确;
B.增大尾气排放口,对反应速率和平衡不产生影响,故B错误;
C.升高排气管温度,温度升高,平衡左移,不利于NOx转化,故C错误;
D.添加合适的催化剂,加快化学反应速率,故D正确;
故答案为:AD.
点评 本题考查较为综合,涉及反应热的计算、反应自发性的判断、化学反应速率和化学平衡的影响因素与图象的关系、平衡常数的计算等知识,为高频考点,其中(4)③是难点,题目难度中等.

| A. | 具有下列电子排布式的原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4 原子半径最大的是① | |
| B. | 具有下列价电子排布式的原子中,①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4第一电离能最大的是④ | |
| C. | ①Na、K、Rb ②N、P、As ③O、S、Se ④Na、P、Cl,元素的电负性随原子序数增大而递增的是④ | |
| D. | 某元素气态基态原子的逐级电离能(kJ•mol-1)分别为738、1 451、7 733、10 540、13 630、17 995、21 703,当它与氯气反应时可能生成的阳离子是X3+ |
| A. | a→b→e→c→d | B. | b→e→a→d→c | C. | a→e→b→c→d | D. | a→d→b→e→c |