题目内容
下列电子式书写错误的是( )
A、 |
B、 |
C、[ H]- H]- |
D、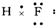 |
考点:电子式
专题:
分析:A、二氧化碳中C分别与两个O形成两对共价键;
B、氮气分子中存在氮氮三键,存在3对共用电子对;
C、氢氧根为带1个负电荷的阴离子,用中括号,并标明所带的电子数;
D、HF为共价化合物,H与F形成1对共价键,F最外层满足8个电子的稳定结构,据此解答即可.
B、氮气分子中存在氮氮三键,存在3对共用电子对;
C、氢氧根为带1个负电荷的阴离子,用中括号,并标明所带的电子数;
D、HF为共价化合物,H与F形成1对共价键,F最外层满足8个电子的稳定结构,据此解答即可.
解答:
解:A、CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ,故A错误;
,故A错误;
B、氮气分子中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气正确的电子式为 ,故B正确;
,故B正确;
C、氢氧根为带1个负电荷的阴离子,用中括号,并标明所带的电子数,故C正确;
D、HF为共价化合物,H与F形成1对共价键,故D正确,
故选A.
 ,故A错误;
,故A错误;B、氮气分子中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气正确的电子式为
 ,故B正确;
,故B正确;C、氢氧根为带1个负电荷的阴离子,用中括号,并标明所带的电子数,故C正确;
D、HF为共价化合物,H与F形成1对共价键,故D正确,
故选A.
点评:本题考查了电子式的判断,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,注意掌握电子式的概念及正确的表示方法.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
如图所示各烧杯中盛有海水,铁在其中被腐蚀,腐蚀的速率由快到慢的顺序为( )


| A、⑤②①③④ |
| B、④③①②⑤ |
| C、③②④①⑤ |
| D、⑤④②①③ |
元素在周期表中的位置取决于( )
| A、元素的核电荷数 |
| B、元素的化合价 |
| C、元素原子的电子层数 |
| D、元素原子的最外层电子数 |
将2mL0.5mol?L-1NaOH溶液加水稀释到100mL,稀释后溶液中NaOH的物质的量浓度为( )
| A、0.1mol?L-1 |
| B、0.01mol?L-1 |
| C、0.2mol?L-1 |
| D、0.02mol?L-1 |
下列热化学方程式或离子方程式中,正确的是( )
| A、甲烷的标准燃烧热为-890.3kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ?mol-1 | ||||
B、500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)
| ||||
| C、氯化镁溶液与氨水反应:Mg2++2OH-═Mg(OH)2↓ | ||||
| D、氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O═2Al(OH)4- |
下列物质属于有机物的是( )
| A、氰化钾(KCN) |
| B、氰酸铵(NH4CNO) |
| C、尿素(NH2CONH2) |
| D、碳化硅(SiC) |
工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=a kJ/mol 在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化数据如下表:下列说法不正确的是( )
| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
| A、10 min内,T1时CH4的化学反应速率比T2时小 |
| B、温度:T1<T2 |
| C、a<0 |
| D、平衡常数:K(T1)<K(T2) |
