题目内容
10.常温下,将下列物质溶于水中分别配制成0.1 mol•L-1溶液,所得溶液PH大于7的是( )| A. | NaCl | B. | HCl | C. | NaOH | D. | H2SO4 |
分析 当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性;据此结合常见化学物质的酸碱性进行分析判断即可.
解答 解:A.NaCl溶于水形成氯化钠溶液,氯化钠溶液显中性,pH等于7,故A错误;
B.HCl溶于水形成盐酸,盐酸显酸性,pH小于7,故B错误;
C.NaOH溶于水形成氢氧化钠溶液,氢氧化钠溶液显碱性,pH大于7,故C正确;
D.H2SO4溶于水得到H2SO4溶液,显酸性,pH小于7,故D错误.
故选C.
点评 本题难度不大,掌握常见化学物质的酸碱性、溶液的酸碱性和溶液pH大小之间的关系是顺利解题的关键.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
20.某些化学键的键能数据如下表:
反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)的焓变△H=-178kJ/mol,△S<0(填>,<,=)
| 化学键 | C-C | C-H | H-H | C-O | C=O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 750 | 463 |
18.根据表中键能数据.计算反应HC1(g)=$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)的△H=+91.5kJ/mol.
| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能 | 436 | 243 | 431 |
5.下列分子属于非极性分子的是( )
| A. | H2S | B. | CO2 | C. | NH3 | D. | H2O |
15.如图是从元素周期表中截取下来的,A、B、C为短周期主族元素,下列说法中正确的是( )
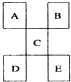

| A. | D一定足金属元素,其金属性比C强 | |
| B. | C的最高价氧化物水化物显强酸性 | |
| C. | E的原子序数一定是A的5倍,且原予半径比A大 | |
| D. | B的氢化物是以分子形式存在,且分子间存在氢键 |
19.已知可逆反应:N2(g)+3H2(g)?2NH3(g),下列关于此反应的说法中错误的是( )
| A. | 增大N2的浓度可使该反应的反应速率加快 | |
| B. | 升高温度,该反应的反应速率加快 | |
| C. | 将1 mol N2和3 mol H2混合进行反应,反应完成时得到2 mol NH3 | |
| D. | 单位时间内生成1 mol N2,同时消耗3 mol H2,说明该反应达到平衡状态 |
20.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 医学上,血液透析是利用了胶体的渗析原理 | |
| B. | 碳酸氢钠可用于制备纯碱,作治疗胃酸过多的药物及食品发酵剂 | |
| C. | 高铁车厢大部分材料采用铝合金,因铝合金强度大、质量轻、抗腐蚀能力强 | |
| D. | 铜的金属性比铝弱,可以用铜罐贮运浓硝酸 |