��Ŀ����
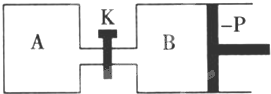
��Լ100��ǰ���¹���ѧ�ҹ�����F��Haber����ʼ�о��ɵ����������ϳɰ���һ�ֹ�ҵ�ϳɰ��ļ�������ͼ��ͼ1���£�
��1����Ȼ���е�H2S���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ������д��������Ӧ�Ļ�ѧ����ʽ�� ��
��2����ҵ�Ͽ������ΪK2O?M2O3?2RO2?nH2O�������ϴ�����ijЩ���ʵ�ԭ��������
��֪Ԫ��M��R��λ��Ԫ�����ڱ��е�3���ڣ�����Ԫ��ԭ�ӵ�������֮��Ϊ27��Rԭ�Ӻ�������� �ֲ�ͬ�˶�״̬��������p������ ����������
��3�������£�������M���ʷ�����Ӧ���� ������ţ�
a��CuSO4��Һ b��Fe2O3c��Ũ���� d��NaOH��Һ e��Na2CO3����
�������������ԭ�����£�
��CH4��g��+H2O��g��?CO��g��+3H2��g��-206.4kJ
��CO��g��+H2O��g��?CO2��g��+H2��g��+41.2kJ��
��4�����ڷ�Ӧ�٣�һ���������ƽ����ϵ��H2�ٷֺ��������ܼӿ췴Ӧ���ʵĴ�ʩ�� ��
a�������¶ȡ����������� ��b������ˮ����Ũ��
c���������d������ѹǿ��
��5�����÷�Ӧ�ڣ���CO��һ��ת���������H2��������1mol CO��H2�Ļ�����壨CO���������Ϊ20%����H2O��Ӧ���õ�1.18mol CO��CO2��H2�Ļ�����壬��COת����Ϊ ��
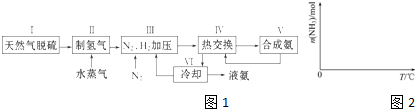
��6�������¶ȶԺϳɰ���Ӧ��Ӱ�죬����ͼ2����ϵ�У�����һ�������µ��ܱ������ڣ���ͨ��ԭ������ʼ�����¶Ȳ������ߣ�NH3���ʵ����仯������ʾ��ͼ��

��1����Ȼ���е�H2S���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ������д��������Ӧ�Ļ�ѧ����ʽ��
��2����ҵ�Ͽ������ΪK2O?M2O3?2RO2?nH2O�������ϴ�����ijЩ���ʵ�ԭ��������
��֪Ԫ��M��R��λ��Ԫ�����ڱ��е�3���ڣ�����Ԫ��ԭ�ӵ�������֮��Ϊ27��Rԭ�Ӻ��������
��3�������£�������M���ʷ�����Ӧ����
a��CuSO4��Һ b��Fe2O3c��Ũ���� d��NaOH��Һ e��Na2CO3����
�������������ԭ�����£�
��CH4��g��+H2O��g��?CO��g��+3H2��g��-206.4kJ
��CO��g��+H2O��g��?CO2��g��+H2��g��+41.2kJ��
��4�����ڷ�Ӧ�٣�һ���������ƽ����ϵ��H2�ٷֺ��������ܼӿ췴Ӧ���ʵĴ�ʩ��
a�������¶ȡ����������� ��b������ˮ����Ũ��
c���������d������ѹǿ��
��5�����÷�Ӧ�ڣ���CO��һ��ת���������H2��������1mol CO��H2�Ļ�����壨CO���������Ϊ20%����H2O��Ӧ���õ�1.18mol CO��CO2��H2�Ļ�����壬��COת����Ϊ
��6�������¶ȶԺϳɰ���Ӧ��Ӱ�죬����ͼ2����ϵ�У�����һ�������µ��ܱ������ڣ���ͨ��ԭ������ʼ�����¶Ȳ������ߣ�NH3���ʵ����仯������ʾ��ͼ��
���㣺��ҵ�ϳɰ�
ר�⣺��ѧӦ��
��������1��H2S���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ��������Ӧ����������һˮ�ϰ�������ԭ���غ�͵����غ���ƽ��д��ѧ����ʽ��
��2��MΪ+3�ۣ�RΪ+4�ۣ���Ϊ��������Ԫ�أ���MΪAl��RΪSi��Si��������Ϊ14����ͬ�����˶�״̬��ͬ�����������Ų�ͼΪ��3s23p2������3p�����������������ͬ��
��3��MΪAl���л�ԭ�ԣ�������������Ե����ʷ�����Ӧ��
��4����Ӧ�������������������ȷ�Ӧ��һ���������ƽ����ϵ��H2�ٷֺ�����˵��ƽ��������У����ܼӿ췴Ӧ���ʣ�˵��Ӱ�췴Ӧ���ʵ��������������¡���ѹ������Ũ�ȵȣ�������Ӧ������֪��Ӧ��������ҷ�Ӧ���������ֻ������ƽ�������ȷ�Ӧ���У�ƽ��������з�Ӧ������������ƽ���ƶ�ԭ����Ӱ�췴Ӧ�������ط����жϣ�
��5�����ݻ�ѧƽ������ʽ��ʽ���㣬ת����=
��100%���㣻
��6���ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ����ʼ��Ӧ���������ʵ������ﵽƽ��״̬���������£�ƽ��������У��������ʵ�����С���ݴ˻����仯ͼ��
��2��MΪ+3�ۣ�RΪ+4�ۣ���Ϊ��������Ԫ�أ���MΪAl��RΪSi��Si��������Ϊ14����ͬ�����˶�״̬��ͬ�����������Ų�ͼΪ��3s23p2������3p�����������������ͬ��
��3��MΪAl���л�ԭ�ԣ�������������Ե����ʷ�����Ӧ��
��4����Ӧ�������������������ȷ�Ӧ��һ���������ƽ����ϵ��H2�ٷֺ�����˵��ƽ��������У����ܼӿ췴Ӧ���ʣ�˵��Ӱ�췴Ӧ���ʵ��������������¡���ѹ������Ũ�ȵȣ�������Ӧ������֪��Ӧ��������ҷ�Ӧ���������ֻ������ƽ�������ȷ�Ӧ���У�ƽ��������з�Ӧ������������ƽ���ƶ�ԭ����Ӱ�췴Ӧ�������ط����жϣ�
��5�����ݻ�ѧƽ������ʽ��ʽ���㣬ת����=
| ������ |
| ��ʼ�� |
��6���ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ����ʼ��Ӧ���������ʵ������ﵽƽ��״̬���������£�ƽ��������У��������ʵ�����С���ݴ˻����仯ͼ��
���
�⣺��1��H2S���ʳ��ð�ˮ���գ�����ΪNH4HS��һ����������NH4HS��Һ��ͨ��������õ�������ʹ����Һ��������Ӧ����������һˮ�ϰ�������ԭ���غ�͵����غ���ƽ��д��ѧ����ʽΪ��2NH4HS+O2
2NH3?H2O+2S��
�ʴ�Ϊ��2NH4HS+O2
2NH3?H2O+2S����
��2����MΪ+3�ۣ�RΪ+4�ۣ���Ϊ��������Ԫ�أ�
��MΪAl��RΪSi��Si��������Ϊ14��������3�����Ӳ㣬�������4�����ӣ�Si��������Ϊ14����ͬ�����˶�״̬��ͬ�����������Ų�ͼΪ��3s23p2������3p�����������������ͬ���ʴ�Ϊ��14��һ��
��3��MΪAl���л�ԭ�ԣ�������������Ե����ʷ�����Ӧ����a��c��������d��NaOH��Һ��Ӧ����������������������������Ӧ����̼���Ʋ���Ӧ���ʴ�Ϊ��be��
��4����Ӧ��CH4��g��+H2O��g��?CO2��g��+3H2��g����H=+206.4 kJ?mol-1�������������������ȷ�Ӧ��һ���������ƽ����ϵ��H2�ٷֺ�����˵��ƽ��������У����ܼӿ췴Ӧ���ʣ�˵��Ӱ�췴Ӧ���ʵ��������������¡���ѹ������Ũ�ȵȣ�������Ӧ������֪��Ӧ��������ҷ�Ӧ���������ֻ������ƽ�������ȷ�Ӧ���У�ƽ��������з�Ӧ��������
a����Ӧ�����ȷ�Ӧ�������¶ȣ���Ӧ��������ƽ��������У�ƽ����ϵ��H2�ٷֺ�������a���ϣ�
b������ˮ����Ũ�ȣ�ƽ��������У���Ӧ��������ƽ����ϵ��H2�ٷֺ�����һ������b�����ϣ�
c������������ı䷴Ӧ���ʲ��ı仯ѧƽ�⣬��Ӧ�������������ٷֺ������䣬��c�����ϣ�
d������ѹǿ����Ӧ���ʼ�С��ƽ��������У������ٷֺ�����С����d�����ϣ�
��ѡa��
��5�����÷�Ӧ�ڣ���CO��һ��ת���������H2��������1mol CO��H2�Ļ�����壨CO���������Ϊ20%���� COΪ0.2mol��H2�����ʵ���Ϊ0.8mol����H2O��Ӧ���õ�1.18mol CO��CO2��H2�Ļ�����壬���ݷ�Ӧǰ������������䣬���ӵIJ���Ӧ������ʼ��ˮ���������ʵ���Ϊ0.18mol����ת����һ����̼�����ʵ���Ϊx�����ݻ�ѧƽ������ʽ��ʽ����
CO��g��+H2O��g��?CO2��g��+H2��g����H=-41.2 kJ?mol-1
��ʼ����mol�� 0.2 0.18+x 0 0.8
�仯����mol�� x x x x
ƽ������mol��0.2-x 0.18 x x+0.8
��0.2-x+x+x+0.8=1.18
x=0.18
��COת����Ϊ
��100%=90%���ʴ�Ϊ��90%��
��6���ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ����ʼ��Ӧ���������ʵ������ﵽƽ��״̬���������£�ƽ��������У��������ʵ�����С��������ͼ��Ϊ��
 ��
��
�ʴ�Ϊ�� ��
��
| ||
�ʴ�Ϊ��2NH4HS+O2
| ||
��2����MΪ+3�ۣ�RΪ+4�ۣ���Ϊ��������Ԫ�أ�
��MΪAl��RΪSi��Si��������Ϊ14��������3�����Ӳ㣬�������4�����ӣ�Si��������Ϊ14����ͬ�����˶�״̬��ͬ�����������Ų�ͼΪ��3s23p2������3p�����������������ͬ���ʴ�Ϊ��14��һ��
��3��MΪAl���л�ԭ�ԣ�������������Ե����ʷ�����Ӧ����a��c��������d��NaOH��Һ��Ӧ����������������������������Ӧ����̼���Ʋ���Ӧ���ʴ�Ϊ��be��
��4����Ӧ��CH4��g��+H2O��g��?CO2��g��+3H2��g����H=+206.4 kJ?mol-1�������������������ȷ�Ӧ��һ���������ƽ����ϵ��H2�ٷֺ�����˵��ƽ��������У����ܼӿ췴Ӧ���ʣ�˵��Ӱ�췴Ӧ���ʵ��������������¡���ѹ������Ũ�ȵȣ�������Ӧ������֪��Ӧ��������ҷ�Ӧ���������ֻ������ƽ�������ȷ�Ӧ���У�ƽ��������з�Ӧ��������
a����Ӧ�����ȷ�Ӧ�������¶ȣ���Ӧ��������ƽ��������У�ƽ����ϵ��H2�ٷֺ�������a���ϣ�
b������ˮ����Ũ�ȣ�ƽ��������У���Ӧ��������ƽ����ϵ��H2�ٷֺ�����һ������b�����ϣ�
c������������ı䷴Ӧ���ʲ��ı仯ѧƽ�⣬��Ӧ�������������ٷֺ������䣬��c�����ϣ�
d������ѹǿ����Ӧ���ʼ�С��ƽ��������У������ٷֺ�����С����d�����ϣ�
��ѡa��
��5�����÷�Ӧ�ڣ���CO��һ��ת���������H2��������1mol CO��H2�Ļ�����壨CO���������Ϊ20%���� COΪ0.2mol��H2�����ʵ���Ϊ0.8mol����H2O��Ӧ���õ�1.18mol CO��CO2��H2�Ļ�����壬���ݷ�Ӧǰ������������䣬���ӵIJ���Ӧ������ʼ��ˮ���������ʵ���Ϊ0.18mol����ת����һ����̼�����ʵ���Ϊx�����ݻ�ѧƽ������ʽ��ʽ����
CO��g��+H2O��g��?CO2��g��+H2��g����H=-41.2 kJ?mol-1
��ʼ����mol�� 0.2 0.18+x 0 0.8
�仯����mol�� x x x x
ƽ������mol��0.2-x 0.18 x x+0.8
��0.2-x+x+x+0.8=1.18
x=0.18
��COת����Ϊ
| 0.18mol |
| 0.2mol |
��6���ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ����ʼ��Ӧ���������ʵ������ﵽƽ��״̬���������£�ƽ��������У��������ʵ�����С��������ͼ��Ϊ��
 ��
���ʴ�Ϊ��
 ��
��
���������⿼���˻�ѧƽ��Ӱ�����ط�����ƽ�����Ӧ�ã�ע�ⷴӦ�����ļ���Ӧ�ã�ͼ����ƣ����ջ����ǹؼ�����Ŀ�ѶȽϴ�

��ϰ��ϵ�д�
�����Ŀ
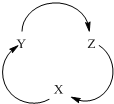 ���и������У���������ͼһ��ת����ϵ��ѡ���ǣ�������
���и������У���������ͼһ��ת����ϵ��ѡ���ǣ�������| ѡ�� | X | Y | Z |
| A | Na2O2 | NaOH | Na2CO3 |
| B | H2SO4 | SO2 | SO3 |
| C | H2SiO3 | SiO2 | Na2SiO3 |
| D | C2H5Br | CH2=CH2 | C2H5OH |
| A��A | B��B | C��C | D��D |
���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�������
| A��Fe3O4��ϡ���ᷴӦ��Fe3O4+8H+=Fe2++2Fe3++4H2O | ||||
| B��Na2S��Һ�ʼ��ԣ�S2-+H2O?HS-+OH- | ||||
C���ö��Ե缫��ⱥ���Ȼ�����Һ��2Cl-+2H+
| ||||
| D��Ca��HCO3��2�����Ca��OH��2��Һ��Ӧ��Ca2++2HCO3-+2OH-=CaCO3��+CO32-+2H2O |
����һ������ˮ��Һ�����ܺ������������е������֣�K+��NH4+��Ba2+��CO32-��Cl-��SO42--����ȡ����200mL��Һ��������ʵ�飺�ٵ�һ�ݼ�����NaOH��Һ�����ȣ��ռ�������1.36g���ڵڶ��ݼ�����BaCl2��Һ�ø������12.54g������������ϴ�ӡ������������Ϊ4.66g����������ʵ�飬�����Ʋ���ȷ���ǣ�������
| A��һ������K+��NH4+��CO32-��SO42-��һ��������Ba2+��Cl- |
| B��һ������NH4+��Cl-��CO32-��SO42-�����ܴ���K+ |
| C��c��SO42-��=0.2mol?L-1��c��NH4+����c��SO42-�� |
| D�������Һ�д���NH4+��Cl-��CO32-��SO42-��K+�������ӣ���c��K+����0.2mol?L-1 |