题目内容
18.下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.086 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | L、R形成的简单离子核外电子数相等 | |
| B. | 单质与浓度相等的稀盐酸反应的速率为Q>L | |
| C. | 氢化物的稳定性为H2T<H2R | |
| D. | M与T形成的化合物既能与强酸反应又能与强碱反应 |
分析 L和Q的化合价都为+2价,应为周期表第ⅡA族,根据半径关系可知Q为Be,L为Mg;R和T的化合价都有-2价,应为周期表第ⅥA族元素,R的最高价为+6价,应为S元素,T无正价,应为O元素;M的化合价为+3价,应为周期表第ⅢA族元素,根据M原子半径大于R小于L可知应和L同周期,为Al元素,结合元素周期律知识解答该题.
解答 解:由上述分析可知,L为Mg,M为Al,Q为Be,R为S,T为O,
A.L、R形成的简单离子核外电子数分别为10、16,故A错误;
B.金属性Mg>Be,则Mg与酸反应越剧烈,则相同条件下单质与稀盐酸反应速率为Q<L,故B错误;
C.非金属性O>S,非金属性越强,氢化物越稳定,所以氢化物的稳定性为H2T>H2R,故C错误;
D.M与T形成的化合物是氧化铝,氧化铝是两性氧化物,溶于强酸、强碱,故D正确;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的化合价、原子半径来推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
5.下列物质间相互发生反应时:①Na+O2②Fe+O2③AgNO3溶液+氨水④HCOOH+Cu(OH)2 ⑤KI溶液+AgNO3溶液 ⑥ ⑦Na2CO3+C6H5COOH ⑧AlCl3+KOH ⑨P+Cl2⑩Cu+HNO3;在不同条件下得到不同产物的是( )
⑦Na2CO3+C6H5COOH ⑧AlCl3+KOH ⑨P+Cl2⑩Cu+HNO3;在不同条件下得到不同产物的是( )
 ⑦Na2CO3+C6H5COOH ⑧AlCl3+KOH ⑨P+Cl2⑩Cu+HNO3;在不同条件下得到不同产物的是( )
⑦Na2CO3+C6H5COOH ⑧AlCl3+KOH ⑨P+Cl2⑩Cu+HNO3;在不同条件下得到不同产物的是( )| A. | 除⑤ | B. | 除②⑤ | C. | 除④⑥ | D. | 除④⑤⑥ |
9.下列物质能发生消去反应,但不能发生催化氧化反应的是( )
| A. |  | B. | (CH3)2CHOH | ||
| C. | CH3CH2C(CH3)2CH2OH | D. | CH3CH2C(CH3)2OH |
13.下列叙述正确的是( )
| A. | 分子式相同的有机物一定是同种物质 | |
| B. | 通式相同的不同物质一定属于同系物 | |
| C. | 相对分子质量相同的不同物质一定是同分异构体 | |
| D. | 同分异构体之间的转化一定是化学变化 |
3.下列各项化学用语中表示正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | CH4分子的比例模型 | ||
| C. | 硫离子的结构示意图: | D. | 氮气的电子式 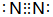 |
10.下列叙述正确的是( )
| A. | 乙烯和聚氯乙烯都能使溴的四氯化碳溶液褪色 | |
| B. | 乙烷、丙烷、丁烷都没有同分异构体 | |
| C. | 酒越陈越香与酯化反应有关 | |
| D. | 甲烷与足量氯气在光照下反应可生成难溶于水的油状液体 |
7.有关化学用语正确的是( )
| A. | 乙烯的结构式C2H4 | B. | 正丁烷的结构简式CH3CH2CH2CH3 | ||
| C. | 四氯化碳的电子式 | D. | 苯的分子式 |
8. 脱落酸具有催熟作用,可延长鲜花盛开时间,脱落酸的结构简式如图所示,下列说法不正确的是( )
脱落酸具有催熟作用,可延长鲜花盛开时间,脱落酸的结构简式如图所示,下列说法不正确的是( )
 脱落酸具有催熟作用,可延长鲜花盛开时间,脱落酸的结构简式如图所示,下列说法不正确的是( )
脱落酸具有催熟作用,可延长鲜花盛开时间,脱落酸的结构简式如图所示,下列说法不正确的是( )| A. | 脱落酸在一定条件下能和乙酸发生酯化反应 | |
| B. | 脱落酸分子中含有4个甲基 | |
| C. | 等量脱落酸与足量的NaHCO3、Na反应,放出CO2与H2的物质的量之比为n(CO2):n(H2)=2:1 | |
| D. | 脱落酸能使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色 |
 .
.