题目内容
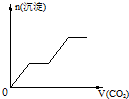
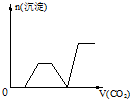
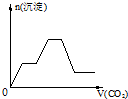
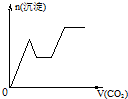
已知Ba(AlO2)2可溶于水,图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述正确的是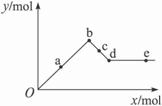
- A.b点时沉淀的物质的量:Al(OH)3>BaSO4
- B.c点时溶液中离子的物质的量:
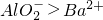
- C.a-b时沉淀的物质的量:BaSO4可能小于Al(OH)3
- D.d-e时溶液中离子的物质的量:Ba2+等于OH-
B
分析:A、根据b点时,沉淀的物质的量最大以及所发生的反应来回答;
B、b~d中Al(OH)3沉淀逐渐溶解转化为Ba(AlO2)2,据此来分析;
C、根据整个过程中离子之间的反应以及用量来确定沉淀的量的多少;
D、当加入的Ba(OH)2的物质的量等于Ba(AlO2)2的物质的量时,溶液中Ba2+与OH-的量相等.
解答:A、在b点时发生反应A12(SO4)3+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓,淀的物质的量:Al(OH)3<BaSO4,故A错误;
B、b点是沉淀的最大值,b~d中Al(OH)3沉淀逐渐溶解转化为Ba(AlO2)2,b~c可以看成是发生反应2Al(OH)3+Ba(OH)2=Ba(AlO2)2+4H2O,所以离子的物质的量AlO2->Ba2+,故B正确;
C、假设有1molA12(SO4)3则溶液中含有2molA13+、3molSO42-,向溶液中逐滴加入Ba(OH)2溶液时发生的反应为:Al3++3OH-=Al(OH)3↓、SO42-+Ba2+=BaSO4↓,则当2molA13+完全沉淀时,消耗Ba(OH)23mol,此时3molSO42-全部沉淀;生成沉淀为2molAl(OH)3和3molBaSO4共5mol,因此,在整个反应过程中BaSO4的物质的量始终大于Al(OH)3的物质的量,故C错误;
D、d~e段中,某点时当加入的Ba(OH)2的物质的量等于Ba(AlO2)2的物质的量时,溶液中Ba2+与OH-的量相等,但d~e段OH-的量多,故D错误.
故选B.
点评:本题考查学生离子之间的反应知识,结合图象知识来考查,增加了难度,熟悉每一段图中对应的化学反应是解答本题的关键.
分析:A、根据b点时,沉淀的物质的量最大以及所发生的反应来回答;
B、b~d中Al(OH)3沉淀逐渐溶解转化为Ba(AlO2)2,据此来分析;
C、根据整个过程中离子之间的反应以及用量来确定沉淀的量的多少;
D、当加入的Ba(OH)2的物质的量等于Ba(AlO2)2的物质的量时,溶液中Ba2+与OH-的量相等.
解答:A、在b点时发生反应A12(SO4)3+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓,淀的物质的量:Al(OH)3<BaSO4,故A错误;
B、b点是沉淀的最大值,b~d中Al(OH)3沉淀逐渐溶解转化为Ba(AlO2)2,b~c可以看成是发生反应2Al(OH)3+Ba(OH)2=Ba(AlO2)2+4H2O,所以离子的物质的量AlO2->Ba2+,故B正确;
C、假设有1molA12(SO4)3则溶液中含有2molA13+、3molSO42-,向溶液中逐滴加入Ba(OH)2溶液时发生的反应为:Al3++3OH-=Al(OH)3↓、SO42-+Ba2+=BaSO4↓,则当2molA13+完全沉淀时,消耗Ba(OH)23mol,此时3molSO42-全部沉淀;生成沉淀为2molAl(OH)3和3molBaSO4共5mol,因此,在整个反应过程中BaSO4的物质的量始终大于Al(OH)3的物质的量,故C错误;
D、d~e段中,某点时当加入的Ba(OH)2的物质的量等于Ba(AlO2)2的物质的量时,溶液中Ba2+与OH-的量相等,但d~e段OH-的量多,故D错误.
故选B.
点评:本题考查学生离子之间的反应知识,结合图象知识来考查,增加了难度,熟悉每一段图中对应的化学反应是解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 已知Ba(AlO2)2可溶于水,图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述正确的是( )
已知Ba(AlO2)2可溶于水,图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述正确的是( )| A、b点时沉淀的物质的量:Al(OH)3>BaSO4 | B、c点时溶液中离子的物质的量:AlO2->Ba2+ | C、a-b时沉淀的物质的量:BaSO4可能小于Al(OH)3 | D、d-e时溶液中离子的物质的量:Ba2+等于OH- |
 已知Ba(AlO2)2可溶于水.如图表示的是向含A12(SO4)30.01mol的溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系(其中a、c分别是0b段和bd段的中点).下列有关叙述正确的是( )
已知Ba(AlO2)2可溶于水.如图表示的是向含A12(SO4)30.01mol的溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系(其中a、c分别是0b段和bd段的中点).下列有关叙述正确的是( ) (2010?金华模拟)已知Ba(AlO2)2可溶于水.如右下图是向100mL 0.02mol?L-1KAl(SO4)2溶液中逐滴加入0.05mol?L-1Ba(OH)2溶液时(25℃),生成沉淀的物质的量与加入Ba(OH)2溶液的体积的关系.下列说法不正确的是( )
(2010?金华模拟)已知Ba(AlO2)2可溶于水.如右下图是向100mL 0.02mol?L-1KAl(SO4)2溶液中逐滴加入0.05mol?L-1Ba(OH)2溶液时(25℃),生成沉淀的物质的量与加入Ba(OH)2溶液的体积的关系.下列说法不正确的是( ) 已知Ba(AlO2)2可溶于水.如图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述错误的是( )
已知Ba(AlO2)2可溶于水.如图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述错误的是( )