题目内容
6.酸性KMnO4、H2O2、NaClO在生产、生活、卫生医疗中常用作消毒剂,其中H2O2还可用于漂白,是化学实验室里必备的重要氧化试剂.高锰酸钾造成的污渍可用还原性的草酸(H2C2O4)去除,Fe(NO3)3也是重要氧化试剂,下面是对这三种氧化剂性质的探究.(1)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的离子方程式Cu+2H++H2O2=Cu2++2H2O.
(2)取300mL0.3mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是0.048mol.
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色.解释产生这两个过程的原因先由棕黄色变为浅绿色,Fe3+先被SO32-还原成Fe2+,后变为棕黄色的原因是H+与NO3-组成的硝酸将Fe2+氧化成Fe3+.
(4)NaClO具有很强的氧化性,可以和Fe(NO3)3制取具有高效净水功能的Na2FeO4,写出相关的方程式2Fe(NO3)3+3NaClO+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O.
分析 (1)铜片的稀盐酸中加入H2O2后,铜片溶解,发生氧化还原反应生成氯化铜、水;
(2)依据氧化还原反应得失电子守恒规律计算解答;
(3)先由棕黄色变为浅绿色,过一会又变为棕黄色,则Fe3+先被还原后又氧化;(4)NaClO具有很强的氧化性,可以将Fe(NO3)3氧化成Na2FeO4,自身被还原成NaCl,据此书写方程式.
解答 解:(1)浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,发生氧化还原反应生成氯化铜、水,反应的离子方程式为Cu+2H++H2O2=Cu2++2H2O,故答案为:Cu+2H++H2O2=Cu2++2H2O;
(2)300mL 0.3mol/L的KI溶液,碘离子的物质的量为0.09mol,依据题意0.09 mol I-→0.03mol I2+0.03IO3-共转移0.24 mol电子,MnO4-→Mn2+,化合价由+7价降低为+2价,设消耗KMnO4的物质的量为n,由电子守恒得:n×5=0.24mol,解得n=0.048 mol;
故答案为:0.048;
(3)先由棕黄色变为浅绿色,过一会又变为棕黄色,则Fe3+先被还原后又氧化,先变为浅绿色的离子方程式是2Fe3++SO32-+H2O=2Fe2++SO42-+2H+,后变为棕黄色的原因是H+与NO3-组成的硝酸将Fe2+氧化成Fe3+,
故答案为:先由棕黄色变为浅绿色,Fe3+先被SO32-还原成Fe2+,后变为棕黄色的原因是H+与NO3-组成的硝酸将Fe2+氧化成Fe3+;
(4)NaClO具有很强的氧化性,可以将Fe(NO3)3氧化成Na2FeO4,自身被还原成NaCl,则发生的化学方程式为:2Fe(NO3)3+3NaClO+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O,
故答案为:2Fe(NO3)3+3NaClO+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及分析应用能力的考查,题目难度不大.

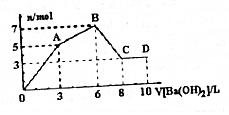 向Al2(SO4)3和AlCl3的混合溶液中逐滴加入1mol/LBa(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所所得沉淀的量的关系如图,下列说法不正确的是( )
向Al2(SO4)3和AlCl3的混合溶液中逐滴加入1mol/LBa(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所所得沉淀的量的关系如图,下列说法不正确的是( )| A. | 图中C点铝元素存在的形式是AlO2- | |
| B. | 原混合溶液中c[Al2(SO4)3]:c(AlCl3)=1:2 | |
| C. | 向D点溶液中通入过量CO2气体,最终将得到9mol沉淀 | |
| D. | OA段反应的离子方程式为:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4 |
①物质的量浓度为0.1mol/L
②物质的量浓度为1mol/L
③含有100mL水
④含有0.1molNaOH.
| A. | ①② | B. | ①③ | C. | ③② | D. | ②④ |
| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | B. | CH2=CH2+H2$→_{△}^{催化剂}$CH3-CH3 | ||
| C. |  +3H2$→_{△}^{Ni}$ +3H2$→_{△}^{Ni}$ | D. |  +HNO3(浓)$\stackrel{浓H_{2}SO_{4}}{→}$ +HNO3(浓)$\stackrel{浓H_{2}SO_{4}}{→}$ NO2+H2O NO2+H2O |
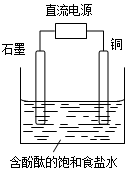
| A. | 石墨电极附近溶液呈红色 | B. | 铜电极上发生还原反应 | ||
| C. | 溶液中的Na+向石墨电极移动 | D. | 铜电极附近观察到黄绿色气体 |
| A. | 苯酚晶体隔绝空气密封保存 | |
| B. | 氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中 | |
| C. | 少量的钠保存在乙醇中 | |
| D. | 新制的氯水通常保存在棕色玻璃试剂瓶中 |