题目内容
下列关于胶体与溶液的说法正确的是( )
| A、向沸水中滴加饱和氯化铁溶液可制得氢氧化铁胶体 |
| B、利用滤纸可以分离胶体与溶液 |
| C、胶体与溶液的本质区别在于能否发生丁达尔效应 |
| D、蔗糖、淀粉、蛋白质的水溶液均能产生丁达尔现象 |
考点:胶体的重要性质
专题:
分析:A.将氯化铁饱和溶液逐滴加入沸水中,制得氢氧化铁胶体溶液;
B.胶体与溶液可透过滤纸;
C.溶液、胶体和浊液这三种分散系的本质的区别在于分散质粒子直径大小;
D.丁达尔现象是胶体特有的性质.
B.胶体与溶液可透过滤纸;
C.溶液、胶体和浊液这三种分散系的本质的区别在于分散质粒子直径大小;
D.丁达尔现象是胶体特有的性质.
解答:
解:A.将氯化铁饱和溶液逐滴加入沸水中,继续加热至呈红褐色,制得氢氧化铁胶体溶液,故A正确;
B.胶体与溶液可透过滤纸,无法分离,故B错误;
C.溶液、胶体和浊液这三种分散系的本质的区别在于分散质粒子直径大小,而不是能否产生丁达尔效应,故C错误;
D.蔗糖溶液无丁达尔效应,故D错误.
故选A.
B.胶体与溶液可透过滤纸,无法分离,故B错误;
C.溶液、胶体和浊液这三种分散系的本质的区别在于分散质粒子直径大小,而不是能否产生丁达尔效应,故C错误;
D.蔗糖溶液无丁达尔效应,故D错误.
故选A.
点评:本题考查学生胶体的性质以及胶体和溶液的区别,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.

练习册系列答案
相关题目
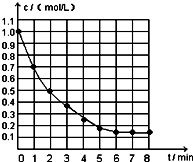 如图表示反应X(g)═4Y(g)+Z(g)△H<0,在某温度时X的浓度
如图表示反应X(g)═4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线.下列有关该反应的描述正确的是( )
| A、该反应的过程是熵减小的过程 |
| B、若降低温度,v正减小,v逆增大 |
| C、第6min后,反应就停止了 |
| D、X在第一分钟和第二分钟内的平均反应速率之比是3:2 |
下列叙述正确的是( )
| A、无论是纯水,还是酸性、碱性或中性稀溶液,在常温下,其c(H+)?c(OH-)=1×10-14 |
| B、c(H+)等于1×10-7mol?L-1的溶液一定是中性溶液 |
| C、0.2 mol?L-1CH3COOH溶液中的c(H+)是0.1 mol?L-1CH3COOH溶液中的c(H+)的2倍 |
| D、任何浓度的溶液都可以用pH来表示其酸性的强弱 |
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图,下列说法正确的是( )
| X | Y |
| Z | W |
| A、非金属性:X<Y<Z |
| B、W的原子序数可能是Y的原子序数的2倍 |
| C、气态氢化物稳定性:Y<W |
| D、Z的化学活泼性一定比X 强 |
设NA是阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol?L-1NaCl溶液含有NA个Na+ |
| B、1.0L浓度为18mol?L-1H2SO4溶液与足量的铜片加热条件下反应,被还原的H2SO4的分子数为9NA |
| C、在酸性条件下,1molFe2+与足量的H2O2溶液反应,转移2NA个电子 |
| D、1molNa与足量O2在一定条件下反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
已知98%的浓H2SO4的密度为1.84g/ml,现将40ml该硫酸用等体积的水进行稀释,所得硫酸的质量分数浓度为( )
| A、等于49% | B、大于49% |
| C、小于49% | D、无法判断 |
下列说法正确的是( )
| A、金属阳离子被还原不一定得到金属单质 |
| B、失电子难的原子获得电子的能力一定强 |
| C、得到电子越多的氧化剂,其氧化性就越强 |
| D、阳离子只有氧化性,阴离子只有还原性 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,11.2L H2O所含分子数为0.5NA |
| B、标准状况下,足量的Fe与2.24 L Cl2反应转移电子的数目为0.3NA |
| C、1mol?L-1 CaCl2溶液中所含Ca2+离子的数目为NA |
| D、通常状况下,32g O2 和O3 的混合物所含的氧原子数一定为2NA |
下列各组物质,按化合物、单质、混合物顺序排列的是( )
| A、生石灰、白磷、冰水混合物 |
| B、烧碱、液氧、碘酒 |
| C、干冰、铁、氯化氢 |
| D、纯碱、氮气、胆矾 |